题目内容
6.amol H2中含有b个氢原子$\frac{a}{4b}$mol-1,则阿伏加德罗常数可以表示为( )| A. | $\frac{b}{2a}$mol-1 | B. | $\frac{a}{4b}$mol-1 | C. | $\frac{a}{b}$mol-1 | D. | $\frac{b}{a}$mol-1 |
分析 根据H原子数求出分子数,根据物质的量、阿伏伽德罗常数与分子数之间的关系式计算.
解答 解:一个H2分子中含有2个H原子,所以含有b个H原子的分子数是$\frac{b}{2}$,NA=$\frac{N}{n}$=$\frac{\frac{b}{2}}{a}$=$\frac{b}{2a}$mol-1,
故选A.
点评 本题考查了物质的量的有关计算,要会运用逆向思维方法解题,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.W、X、Y、Z均为短周期主族元素,原子序数依次增加,且原子核外L电子层的电子数分别为0、5、8、8,它们的最外层电子数之和为18.下列说法正确的是( )
| A. | 单质的沸点:W>X | B. | 氧化物的水化物的酸性:Y<Z | ||
| C. | 阴离子的还原性:Y>Z | D. | X与Y不能存在于同一离子化合物中 |
14.在MgCl2、KCl、K2SO4三种盐的混合溶液中含有0.8mol K+、0.1mol Mg2+、0.4mol Cl-,则该溶液中含SO${\;}_{4}^{2-}$为( )
| A. | 0.1 mol | B. | 0.2 mol | C. | 0.3mol | D. | 0.15 mol |
16.下列叙述的两个量,一定相等的是( )
| A. | 质量相等的金刚石和C60中的碳原子数目 | |
| B. | 0.1 mol/L NaCl溶液与0.05 mol/L Na2CO3溶液中所含Na+的数目 | |
| C. | 标准状况下等体积的SO2和SO3的分子数目 | |
| D. | 同温同压相同体积的两种气体12C18O和14N2的密度 |
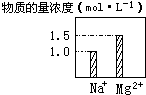 在0.2L NaCl、MgCl2的混合溶液中,部分离子浓度大小如图所示,
在0.2L NaCl、MgCl2的混合溶液中,部分离子浓度大小如图所示,