题目内容
9.下列有关实验装置或实验操作正确的是( ) | 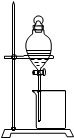 | 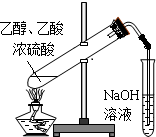 | 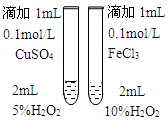 |
| 配制一定物质的量浓度的溶液 | 用CCl4萃取碘水中的碘 | 制备乙酸乙酯 | 比较不同催化剂 对反应速率的影响 |
| A | B | C | D |
| A. | A | B. | B | C. | C | D. | D |
分析 A.转移液体需要使用玻璃棒引流;
B.碘易溶于四氯化碳;
C.乙酸乙酯能与氢氧化钠反应;
D.过氧化氢的浓度不同.
解答 解:A.转移液体需要使用玻璃棒引流,防止液体溅出,故A错误;
B.碘易溶于四氯化碳,四氯化碳与水互不相溶,可做萃取剂,故B正确;
C.乙酸乙酯能与氢氧化钠反应,应用饱和碳酸钠,故C错误;
D.过氧化氢的浓度不同,浓度影响反应速率,则不能探究催化剂对反应速率的影响,故D错误.
故选B.
点评 本题考查化学实验方案的评价,为高频考点,涉及反应速率的影响因素、有机物的性质、物质分离提纯以及溶液配制等,把握反应原理及实验装置的作用为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案
相关题目
1.下列有关说法正确的是( )
| A. | 氢氧燃料电池的能量转换形式仅为化学能转化为电能 | |
| B. | 一定条件下,使用催化剂能加快反应速率但不能改变平衡转化率 | |
| C. | NH4Cl和HCl溶于水后滴加石蕊都变红色,说明它们均能电离出H+ | |
| D. | 在一密闭容器中发生2SO2+O2?2SO3反应,增大压强,平衡会正向移动,$\frac{{c}^{2}(S{O}_{3})}{{c}^{2}(S{O}_{2})•c({O}_{2})}$的值增大 |
20.除去下列物质中的少量杂质(括号内为杂质),所选试剂和分离方法能达到实验目的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 淀粉(氯化钠) | 蒸馏水 | 渗析 |
| B | 乙醇(乙酸) | 生石灰 | 分液 |
| C | 苯(苯酚) | 溴水 | 过滤 |
| D | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
17.绿原酸的结构简式如图,关于绿原酸判断正确的是( )
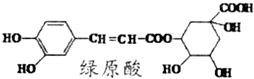
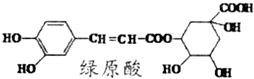
| A. | 分子中所有的碳原子均可能在同一平面内 | |
| B. | 1 mol绿原酸与足量溴水反应,最多消耗2.5mol Br2 | |
| C. | 绿原酸可以与FeCl3溶液发生显色反应 | |
| D. | 绿原酸不能发生消去反应 |
1.甲、乙、丙三种含不相同离子的可溶性强电解质,它们所含的离子如下表所示:
若取等质量的甲、乙、丙配成相同体积的溶液,发现溶质的物质的量浓度c(甲)>c(乙)>c(丙),
则乙物质( )
| 阳离子 | NH4+、Na+、Mg2+ |
| 阴离子 | OH-、NO3-、SO42- |
则乙物质( )
| A. | 可能是Na2S04 | B. | 可能是NH4NO3 | C. | 可能是NaOH | D. | 一定不是(NH4)2SO4 |
18.按图示装置进行电解实验,随着实验进行不会发生改变的是( )
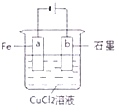

| A. | Cu2+物质的量浓度 | B. | Cl-物质的量浓度 | ||
| C. | a极质量 | D. | b极质量 |
 .
. .
. .
. .
. .
. .
. D.
D. E.
E.