��Ŀ����
����Ŀ��ҩ�ﻪ��Ƭ�����ص�Ƭ��ʹ��˵����IJ����������£� 
��1����������˵������ѧ��ѧ֪ʶ�ش�
����Ƭ�к��еĻ��Գɷ�����д����ʽ����
��2��ijѧ��Ϊ��֤����Ƭ��ȷ�������������Գɷ֣����ʵ�����£�����д��
�ٽ�ҩƬ���顢�ܽ⡢���ˣ�������Һ��װ�ڼס������Թ��б��ã�
���ڼ��Թ��м�������һ���Լ��������ã��۲쵽Һ��ֲ㣬���ϲ�Һ����ɫΪ��ɫ���������Լ�Ϊ�����е�������ĸ�����ɴ�˵�����ڷ��ӵ⣮
A������������Һ B���ƾ� C�����Ȼ�̼ D������
�������Թ��еμ���Һ����Һ����ɫ��Ҳ��˵�����ڷ��ӵ⣮
���𰸡�
��1��I2
��2��C������
���������⣺��1����ҩƷ˵����ָ������Ҫ�ɷ��Ƿ��ӵ⣬�ⵥ�ʣ�����ʽΪ��I2 �� ���Դ��ǣ�I2����2���������ƺ͵ⷴӦ���ɴε����ƺ͵⻯�ƣ����ֲ㣬���������л��ܼ����Ҿƾ���ˮ���ֲ㣬��������Ӧ�����ֲ㣬����CCl4�е��ܽ�ȴ�����ˮ�е��ܽ�ȣ��ҵ���CCl4����Ӧ��ˮ��CCl4�����ܣ�����CCl4����ˮ���²㣻��ȡ�����Ȼ�̼�ܶȴ���۲쵽Һ��ֲ㣬�²���Ϻ�ɫ���ϲ㼸����ɫ�����ݵⵥ�������۱���������������ⵥ�ʣ����Դ��ǣ�C�����ۣ�

����Ŀ���ں��¡����ݵ��ܱ������У��������A��B��C �����ʵ���Ũ��(c)��ʱ��(t) �Ĺ�ϵ���±���ʾ:
t c | ��ʼ | 2min | 4min | 6min | 8min |
c(A)( mol��L -1) | 2.50 | 2.20 | 2.00 | 2.00 | 2.20 |
c(B)( mol��L -1) | 1.56 | 2.16 | 2.56 | 2.56 | 2.16 |
c(C)( mol��L -1) | 0.39 | 0.54 | 0.64 | 0.64 | 1.54 |
�����:
��1��ǰ2 min�ڣ�v(B)= _______________________��
��2�� ��2 minĩA ��ת����Ϊ_________________��
��3���÷�Ӧ�Ļ�ѧ����ʽΪ_______________________________________��
��4��6 min - 8 min��ֻ�ı��˷�Ӧ��ϵ��ijһ�����ʵ�Ũ�ȣ���ӦΪ_____(��ѡ����ĸ)
a.����A��Ũ�� b.��СB��Ũ�� c.����C��Ũ��
������ʵ�Ũ�ȸı���Ϊ________________mol��L -1
��5���������ͬ�����£�����ʼ������������ʵ����ʵ���Ũ����ԭ����2������_____��ԭ����2����
a. B��ƽ��Ũ�� b. �ﵽƽ���ʱ�� c. ƽ��ʱ������ܶ� d. ƽ�ⳣ��
����Ŀ��ij��ҵ��������Ҫ����Al2O3��Co2O3CoO������Fe3O4�Ƚ��������Co2O3CoO����ǿ�Ӧ����ʵ���ҿƼ���Ա����֮���벢�Ʊ�������ʣ�����������£� 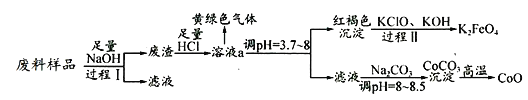
��1�����̢��еIJ���������__��д�����̢�����Ӧ�Ļ�ѧ����ʽ____________��
��2����Һa�к��н��������� _________________��
��3����Һa���ݳ��Ļ���ɫ����������������˵������ȷ����_________��
����������Ư���Ե���������
��Һ�Ⱥ���ˮ��ΪҺ�壬�Ҷ������ȷ���
�۽�����ͨ���Һʱ���������������������ǻ�ԭ��
�ܴ���������ֽ⣬˵��������������
������ˮ�е���������Һ���а�ɫ�������ɣ�˵����ˮ�к�Cl��
��4��д�����̢�����Ӧ�����ӷ���ʽ��_______________________________��
������ص��ܷ�ӦΪ��3Zn+2K2FeO4+8H2O![]() 3Zn��OH��2+2Fe��OH��3+4KOH
3Zn��OH��2+2Fe��OH��3+4KOH
����ʱ������ӦʽΪ___________________________________��
��5��Co�����γ�CoC2O42H2O��MΪ183g/mol����5.49g�þ����ڿ����м��ȣ��ڲ�ͬ�¶��·ֱ�õ�һ�ֹ������ʣ������������
�¶ȷ�Χ���棩 | ����������g�� |
150��210 | 4.41 |
290��320 | 2.41 |
890��920 | 2.25 |
���ⶨ��210�桫290������У�����������ֻ��CO2����˹��̷����Ļ�ѧ��Ӧ����ʽΪ��______________________________________��

