题目内容
在体积为1L的两个恒容密闭容器中,分别充入1molCO和1molH2O(g)的混合气体,进行如下化学反应:CO(g)+H2O(g)?CO2(g)+H2(g),反应物CO的物质的量在不同温度时物质的量随时间的变化如下表所示,回答下列问题:
(1)1100℃时,前10min该反应的化学反应速率v(CO2)=______,830℃平衡后CO转化率的为______.
(2)1100℃时化学平衡常数K=______,该反应为______反应(填“吸热”和“放热”).
(3)能判断该反应是否达到化学平衡状态的依据是______.
(a)容器中压强不变(b)混合气体中c(CO)不变
(c)v逆(H2)=v正(H2O)(d)c(CO2)=c(CO)
(4)1100℃时达到平衡后,若向容器中再充入2molCO和2molH2O(g),平衡______
______移动(选填“向正反应方向”或“向逆反应方向”或“不”),再达到平衡时,H2百分含量______(选填“增大”或“减小”或“不变”).
(5)830℃时,若在体积为2L的密闭容器中充入1molCO2和1molH2的混合气体,60min时反应达平衡状态,画出c(CO)和c(H2)随时间变化而变化的趋势图.
| 0min | 10min | 20min | 30min | 40min | 50min | |
| 830℃ | 1mol | 0.8mol | 0.65mol | 0.55mol | 0.5mol | 0.5mol |
| 1100℃ | 1mol | 0.75mol | 0.6mol | 0.6mol | 0.6mol | 0.6mol |
(2)1100℃时化学平衡常数K=______,该反应为______反应(填“吸热”和“放热”).
(3)能判断该反应是否达到化学平衡状态的依据是______.
(a)容器中压强不变(b)混合气体中c(CO)不变
(c)v逆(H2)=v正(H2O)(d)c(CO2)=c(CO)
(4)1100℃时达到平衡后,若向容器中再充入2molCO和2molH2O(g),平衡______
______移动(选填“向正反应方向”或“向逆反应方向”或“不”),再达到平衡时,H2百分含量______(选填“增大”或“减小”或“不变”).
(5)830℃时,若在体积为2L的密闭容器中充入1molCO2和1molH2的混合气体,60min时反应达平衡状态,画出c(CO)和c(H2)随时间变化而变化的趋势图.

(1)v(CO)=
=
=0.025mol/(L.min),反应方程式中一氧化碳和二氧化碳的计量数相等,所以其反应速率相等,则二氧化碳的反应速率是0.025mol/(L.min),
一氧化碳的转化率=
×100%=
×100%=50%,
故答案为:0.025mol/(L.min);50%;
(2)反应达到平衡状态时,C(CO)=
=0.6mol/L,则一氧化碳反应的物质的量浓度是0.4mol/L,氢气、一氧化碳、二氧化碳和水反应的物质的量浓度相等,所以氢气和二氧化碳的物质的量浓度是0.4mol/L,水的物质的量浓度是0.6mol/L,则K=
=
=
=0.44,
升高温度,一氧化碳的平衡物质的量增大,则平衡向逆反应方向移动,正反应是放热反应,
故答案为:
(或0.44);放热;
(3)(a)该反应是反应前后气体体积不变的化学反应,所以无论反应是否达到平衡状态,容器中压强始终不变,所以不能据此判断平衡状态,故错误;
(b)反应达到平衡状态时,反应体系中各物质的物质的量浓度不变,所以混合气体中c(CO)不变能作为平衡状态的判断依据,故正确;
(c)v逆(H2)=v正(H2O)时,反应达到平衡状态,故正确;
(d)无论反应是否达到平衡状态,c(CO2)与c(CO)都有可能相等,与反应初始浓度和转化率有关,所以不能作为判断平衡状态的依据,故错误;
故选bc;
(4)1100℃时达到平衡后,若向容器中再充入2molCO和2molH2O(g),反应物浓度增大平衡向正反应方向移动,
该反应是一个反应前后气体体积不变的可逆反应,压强对平衡无影响,所以再达到平衡时,H2百分含量不变,
故答案为:向正反应方向;不变;
(5)反应开始时,一氧化碳的浓度为0,氢气的浓度是
=0.5mol/L,随着反应的进行,氢气的浓度逐渐减小,一氧化碳的浓度逐渐增大,当60min时,一氧化碳和氢气的浓度相等,反应达到平衡状态,其图象为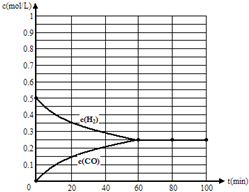 ,
,
故答案为: .
.
| ||
| △t |
| ||
| 40min |
一氧化碳的转化率=
| 反应的CO的物质的量 |
| 反应初始时CO的总的物质的量 |
| (1-0.5)mol |
| 1mol |
故答案为:0.025mol/(L.min);50%;
(2)反应达到平衡状态时,C(CO)=
| 0.6mol |
| 1L |
| C(CO).C(H2O) |
| C(H2).C(CO2) |
| 0.6mol/L×0.6mol/L |
| 0.4mol/L×0.4mol/L |
| 9 |
| 4 |
升高温度,一氧化碳的平衡物质的量增大,则平衡向逆反应方向移动,正反应是放热反应,
故答案为:
| 9 |
| 4 |
(3)(a)该反应是反应前后气体体积不变的化学反应,所以无论反应是否达到平衡状态,容器中压强始终不变,所以不能据此判断平衡状态,故错误;
(b)反应达到平衡状态时,反应体系中各物质的物质的量浓度不变,所以混合气体中c(CO)不变能作为平衡状态的判断依据,故正确;
(c)v逆(H2)=v正(H2O)时,反应达到平衡状态,故正确;
(d)无论反应是否达到平衡状态,c(CO2)与c(CO)都有可能相等,与反应初始浓度和转化率有关,所以不能作为判断平衡状态的依据,故错误;
故选bc;
(4)1100℃时达到平衡后,若向容器中再充入2molCO和2molH2O(g),反应物浓度增大平衡向正反应方向移动,
该反应是一个反应前后气体体积不变的可逆反应,压强对平衡无影响,所以再达到平衡时,H2百分含量不变,
故答案为:向正反应方向;不变;
(5)反应开始时,一氧化碳的浓度为0,氢气的浓度是
| 1mol |
| 2L |
 ,
,故答案为:
 .
.
练习册系列答案
相关题目
 2NH3,用υ(H2)和υ(N2)分别表示其中的化合反应的速率,用υ(NH3)表示其中分解反应的速率。下列能说明反应已达到平衡状态的是( )
2NH3,用υ(H2)和υ(N2)分别表示其中的化合反应的速率,用υ(NH3)表示其中分解反应的速率。下列能说明反应已达到平衡状态的是( ) CO2+H2,达到平衡时,
CO2+H2,达到平衡时,