题目内容
18.已知: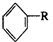 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$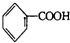
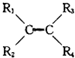 $\stackrel{O_{3}/Zn+H_{2}O}{→}$
$\stackrel{O_{3}/Zn+H_{2}O}{→}$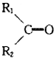 +
+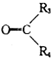 (其中R、R1、R2、R3和R4均表示烃基)今有A~K等11种不同的有机物,它们之间的转化关系如下.其中A为烃,1mol A可得2mol B,E与G为同分异构体.
(其中R、R1、R2、R3和R4均表示烃基)今有A~K等11种不同的有机物,它们之间的转化关系如下.其中A为烃,1mol A可得2mol B,E与G为同分异构体.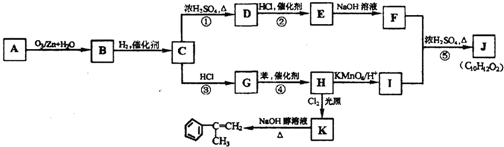
请回答下列问题:
(1)指出反应的类型:①消去反应,②加成反应,③取代反应,④取代反应.
(2)有机物H的结构简式
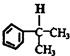 .
.(3)写出反应⑤的化学方程式(有机物写结构简式)
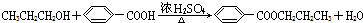 .
.(4)A的结构简式为(CH3)2C=C(CH3)2.A同分异构体中与A具有相同官能团,且与氢气加成后生成2-甲基戊烷的同分异构体有4种.(考虑顺反异构)
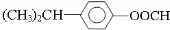
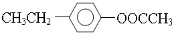
(5)J(C10H12O2)有多种同分异构体.若J中苯环上两个取代基处于对位,一个取代基含-CH3,另外一个取代基含有“-COO-”结构的基团,且1mol J能与含2mol NaOH的溶液完全反应,写出满足上述要求的J的所有可能结构简式
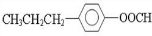 、
、 、
、 、
、 .
.
分析 A为烃,1mol A可得2mol B,根据已知信息可知A分子应该是结构对称的,G与苯反应生成H,H可以最终转化为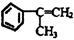 ,这说明G中含有3个碳原子,因此A中应该含有6个碳原子,B能与氢气发生加成反应生成C,C既能与氯化氢发生反应,也能在浓硫酸的作用下发生消去反应生成D,因为D能与氯化氢在催化剂的作用下反应,这说明该反应应该是加成反应,即D中含有碳碳双键,所以C中含有羟基,由于A的结构是对称的,则根据
,这说明G中含有3个碳原子,因此A中应该含有6个碳原子,B能与氢气发生加成反应生成C,C既能与氯化氢发生反应,也能在浓硫酸的作用下发生消去反应生成D,因为D能与氯化氢在催化剂的作用下反应,这说明该反应应该是加成反应,即D中含有碳碳双键,所以C中含有羟基,由于A的结构是对称的,则根据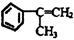 结构可知,A的结构简式应该是(CH3)2C=C(CH3)2,B应该是
结构可知,A的结构简式应该是(CH3)2C=C(CH3)2,B应该是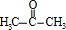 ,C是
,C是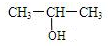 ,D是CH2=CHCH3,E是卤代烃,在氢氧化钠溶液中水解生成F是醇.G是CH3CH(Cl)CH3,G与苯发生取代反应生成H,则H的结构简式为
,D是CH2=CHCH3,E是卤代烃,在氢氧化钠溶液中水解生成F是醇.G是CH3CH(Cl)CH3,G与苯发生取代反应生成H,则H的结构简式为 ,H与氯气发生苯环侧链上氢原子的取代反应,最后再通过卤代烃的消去反应生成
,H与氯气发生苯环侧链上氢原子的取代反应,最后再通过卤代烃的消去反应生成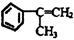 .H被酸性高锰酸钾溶液直接氧化生成I,则I是
.H被酸性高锰酸钾溶液直接氧化生成I,则I是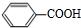 ,由于E与G的分子式相同但结构不同,因此E的结构简式为CH3CH2CH2Cl,则F的结构简式为CH3CH2CH2OH,苯甲酸与F通过酯化反应生成J为
,由于E与G的分子式相同但结构不同,因此E的结构简式为CH3CH2CH2Cl,则F的结构简式为CH3CH2CH2OH,苯甲酸与F通过酯化反应生成J为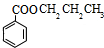 ,据此解答.
,据此解答.
解答 解:A为烃,1mol A可得2mol B,根据已知信息可知A分子应该是结构对称的.G与苯反应生成H,H可以最终转化为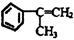 ,这说明G中含有3个碳原子,因此A中应该含有6个碳原子.B能与氢气发生加成反应生成C,C既能与氯化氢发生反应,也能在浓硫酸的作用下发生消去反应生成D,因为D能与氯化氢在催化剂的作用下反应,这说明该反应应该是加成反应,即D中含有碳碳双键,所以C中含有羟基.由于A的结构是对称的,则根据
,这说明G中含有3个碳原子,因此A中应该含有6个碳原子.B能与氢气发生加成反应生成C,C既能与氯化氢发生反应,也能在浓硫酸的作用下发生消去反应生成D,因为D能与氯化氢在催化剂的作用下反应,这说明该反应应该是加成反应,即D中含有碳碳双键,所以C中含有羟基.由于A的结构是对称的,则根据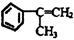 结构可知,A的结构简式应该是(CH3)2C=C(CH3)2,B应该是
结构可知,A的结构简式应该是(CH3)2C=C(CH3)2,B应该是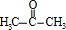 ,C是
,C是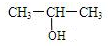 ,D是CH2=CHCH3,E是卤代烃,在氢氧化钠溶液中水解生成F是醇.G是CH3CH(Cl)CH3,G与苯发生取代反应生成H,则H的结构简式为
,D是CH2=CHCH3,E是卤代烃,在氢氧化钠溶液中水解生成F是醇.G是CH3CH(Cl)CH3,G与苯发生取代反应生成H,则H的结构简式为 .H与氯气发生苯环侧链上氢原子的取代反应,最后再通过卤代烃的消去反应生成
.H与氯气发生苯环侧链上氢原子的取代反应,最后再通过卤代烃的消去反应生成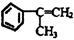 .H被酸性高锰酸钾溶液直接氧化生成I,则I是
.H被酸性高锰酸钾溶液直接氧化生成I,则I是 .由于E与G的分子式相同但结构不同,因此E的结构简式为CH3CH2CH2Cl,则F的结构简式为CH3CH2CH2OH,苯甲酸与F通过酯化反应生成J为
.由于E与G的分子式相同但结构不同,因此E的结构简式为CH3CH2CH2Cl,则F的结构简式为CH3CH2CH2OH,苯甲酸与F通过酯化反应生成J为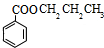 ,
,
(1)根据以上分析可知①②③④分别是消去反应,加成反应,取代反应,取代反应,
故答案为:消去反应、加成反应、取代反应、取代反应;
(2)根据以上分析可知,H的结构简式为 ,
,
故答案为: ;
;
(3)反应⑤是酯化反应,反应的化学方程式为: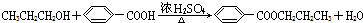
故答案为: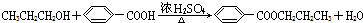 ;
;
(4)根据以上分析可知,A的结构简式为(CH3)2C=C(CH3)2,A同分异构体中与A具有相同官能团,即有碳碳双键,且与氢气加成后生成2-甲基戊烷的同分异构体有(CH3)2C=CHCH2CH3、(CH3)2CHCH=CHCH3(有顺式和反式两种)、(CH3)2CHCH2CH=CH2,所以共有4种,
故答案为:(CH3)2C=C(CH3)2;4;
(5)J(C10H12O2)有多种同分异构体.若J中苯环上只有两个取代基并处于对位,一个取代基含-CH3,另外一个取代基含有“-COO-”结构的基团,且1mol J能与含2mol NaOH的溶液完全反应,这说明分子中应该含有酯基,且酯基水解后又产生1个酚羟基,所以可能的结构简式有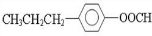 、
、 、
、 、
、 ,
,
故答案为: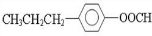 、
、 、
、 、
、 .
.
点评 本题考查有机物推断,注意根据K的消去反应产物结构与反应条件综合分析确定A的结构,注意根据F、G互为同分异构确定F的结构,综合考查学生分析推理能力,需要学生熟练掌握官能团的性质与转化,难度中等.

 名校课堂系列答案
名校课堂系列答案| A. | 7.8 g Na2O2中含有的阴离子数目为0.2NA | |
| B. | 标准状况下,2.24 L CHCl3的分子数为0.1NA | |
| C. | 1 L 0.1 mol/L Al2(SO4)3溶液中,Al3+的数目为0.2NA | |
| D. | 0.1 mol Fe与足量稀HNO3反应,转移电子数为0.3NA |
| A. | AlCl3溶液中通入过量的氨水:Al3++4NH3•H2O=AlO2-+2H2O+4NH4+ | |
| B. | 向NH4HCO3 溶液中加过量NaOH 溶液并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 将Cu片加入稀硝酸中:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O | |
| D. | 向Na2S2O3溶液中加入稀硫酸:2S2O32-+2H+=SO42-+3S↓+H2O |
 从石墨中分离出来的石墨烯是已知最薄、最坚硬的物质,可制成电阻率最小的纳米材料,其结构如图所示.下列关于石墨烯的说法正确的是( )
从石墨中分离出来的石墨烯是已知最薄、最坚硬的物质,可制成电阻率最小的纳米材料,其结构如图所示.下列关于石墨烯的说法正确的是( )| A. | 具有良好的导电性 | B. | 属于高分子化合物 | ||
| C. | 与金刚石互为同位素 | D. | 不能与氧气发生反应 |
| A. | Cu | B. | Fe | C. | SO2 | D. | I- |
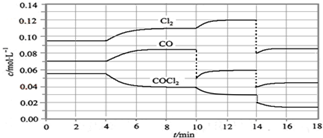
| A. | 从第10 min到第12 min时,生成Cl2的速率v(Cl2)=0.01 mol•L-1•min-1 | |
| B. | 第8 min时与第18 min时反应的平衡常数不相同 | |
| C. | 在第14 min时,改变的条件可能是压缩反应容器的体积 | |
| D. | CO在2-3min、12-13min和16-18min时平均反应速率相等 |
| 甲 | 乙 | 丙 | ||
| 起始物质的量 | n(SO2)/mol | 0.4 | 0.4 | 0.8 |
| n(O2)/mol | 0.24 | 0.48 | 0.48 | |
| SO2的平衡转化率 | 80% | α1 | α2 | |
| A. | 甲中反应的平衡常数大于乙 | B. | 平衡时,SO2的转化率:α1<80%<α2 | ||
| C. | 该温度下,乙中平衡常数值为400 | D. | 平衡时,丙中c(SO3)是甲中的2倍 |
| A. | 乙苯 | B. | 反-2-丁烯 | C. | 环己烷 | D. | 对二甲苯 |
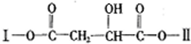 (其中I、II为未知部分的结构)为推测X的分子结构,进行如图的转化:
(其中I、II为未知部分的结构)为推测X的分子结构,进行如图的转化: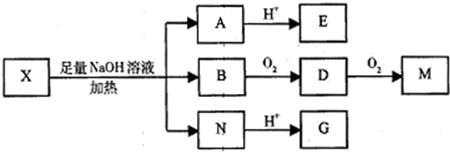
 ;
; ;
;