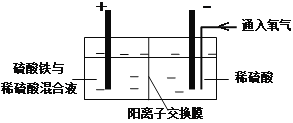
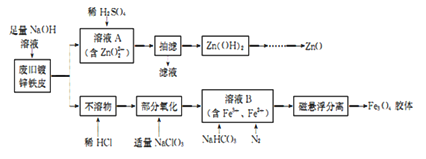
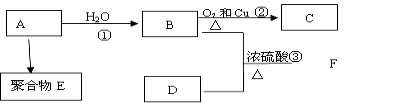
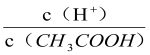题目内容
【题目】当三份铜粉分别与足量的稀硝酸、浓硝酸、热的浓硫酸反应后收集到的气体在相同状况下体积相等时,三份铜粉的质量比为
A. 3:1:2 B. 3:2:2 C. 1:1:2 D. 1:3:2
【答案】A
【解析】当三份铜粉分别与足量的稀硝酸、浓硝酸、热的浓硫酸反应后收集到的气体在相同状况下体积相等时,我们假设所有的气体在标况下都是22.4L,即均是1mol,则
(1)当铜粉与足量的稀硝酸反应,生成1molNO时
3Cu+8HNO3=3 Cu(NO3)2+2NO↑+4H2O
3 2
1.5 1 mol
(2)当铜粉与足量的浓硝酸反应,生成1molNO2时
Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O
1 2
0.5 1 mol
(3)当铜粉与热的浓硫酸反应,生成1molSO2时
Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
1 1
1 1 mol
三份铜粉的质量比为1.5:0.5:1=3:1:2,答案选A。

练习册系列答案
相关题目