题目内容
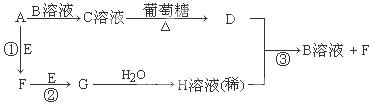
常温下,相同pH的氢氧化钠和醋酸钠溶液加水稀释,平衡时pH随溶液体积变化的曲线如图所示,则


| A.b、c两点溶液的导电能力相同 |
B.c点溶液中 |
| C.a、b、c三点溶液中水的电离程度a>c>b |
D.用相同浓度的盐酸分别与等体积的b、c处溶液反应,消耗盐酸体积 |
C
试题分析:氢氧化钠溶液中的氢氧根离子主要是氢氧化钠电离出来的,氢氧化钠完全电离,体积和pH都相同的氢氧化钠和醋酸钠溶液加水稀释的过程中,NaOH不能继续电离,NaOH溶液中氢氧根离子浓度变化大;水解是微弱的,醋酸钠溶液中醋酸根离子可继续水解,溶液中的氢氧根离子浓度变化小,所以含b点的曲线pH变化是NaOH溶液的,含a、c点的曲线pH变化是醋酸钠溶液的;A、溶液的导电能力和溶液中自由移动离子的浓度有关,b、c两点溶液pH相同,但其他离子浓度不一样,所以导电能力不一样,故A错误;B、c点溶液中,根据质子守恒,得出c(OH-)=c(H+)+c(CH3COO-),故B错误;C、NaOH电离出的氢氧根离子浓度抑制了水的电离,所以b点溶液中水的电离程度最小;水解促进水的电离,由于醋酸钠溶液中的氢氧根离子浓度来自于醋酸根离子水解生成的氢氧根离子,氢氧根离子浓度越大,说明水解程度越大,水的电离程度越大,a点的pH大于c点的pH,说明a点氢氧根离子浓度大于c点氢氧根离子,所以a、c二点溶液水的电离程度a>c,综上所述a、b、c三点溶液水的电离程度a>c>b,故C正确;D、用等浓度NaOH溶液和等体积b、c处溶液反应,c点为醋酸根水解导致溶液呈碱性,c点溶液中醋酸根和氢氧根离子均消耗HCl,而b点只有NaOH消耗盐酸(NaOH完全电离),故消耗HCl溶液体积Vc<Vb,故D错误。

练习册系列答案
相关题目

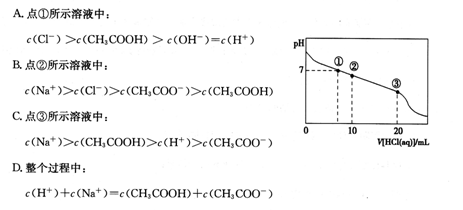
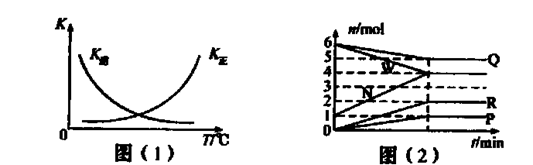
 2G(g)。忽略
2G(g)。忽略