题目内容
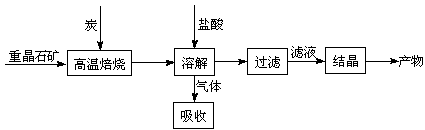
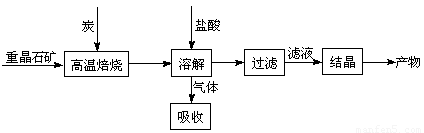
工业上制备BaCl2,有如下过程:
BaSO4(s)+4C(s) 4CO(g)+BaS(s);ΔH1=+571.2 kJ·mol-1①
4CO(g)+BaS(s);ΔH1=+571.2 kJ·mol-1①
BaSO4(s)+2C(s) 2CO2(g)+BaS(s);ΔH2=+226.2 kJ·mol-1②
2CO2(g)+BaS(s);ΔH2=+226.2 kJ·mol-1②
(1)制备过程中会得到硫化钠.Na2S水解的离子方程式为:________.
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,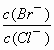 =________.
=________.
[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
(3)反应C(s)+CO2(g) 2CO(g)的ΔH3=________kJ·mol-1.
2CO(g)的ΔH3=________kJ·mol-1.
答案:
解析:
解析:
|
|

练习册系列答案
相关题目

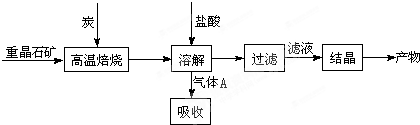
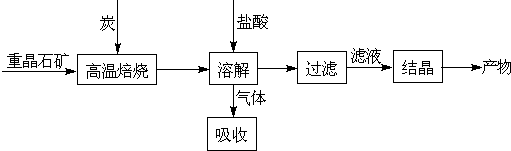
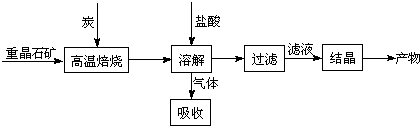
 4CO(g) + BaS(s) △H1 =+571.2 kJ·mol-1 ①
4CO(g) + BaS(s) △H1 =+571.2 kJ·mol-1 ①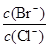 =
。[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
=
。[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]