题目内容
用NA表示阿伏伽德罗常数,下列叙述正确的是
| A.1mol碳正离子( CH5+ )所含的质子数为11NA |
| B.15g乙烷分子中所含非极性共价键数为3NA |
| C.标准状况下,22.4L苯完全燃烧所消耗的氧气分子数为7.5NA |
| D.1L 0.1mol/L乙酸溶液中H+数为0.1NA |
A
解析试题分析:A、碳元素和氢元素的质子数分别是6和1,所以1mol碳正离子( CH5+ )所含的质子数为11NA,A正确;B、乙烷分子中含有1个碳碳单键,属于非极性键。15g乙烷的物质的量=15g÷30g/mol=0.5mol,因此15g乙烷分子中所含非极性共价键数为0.5NA,B不正确;C、标准状况下,苯不是气体,不能适用于气体摩尔体积,因此标准状况下,22.4L苯完全燃烧所消耗的氧气分子数一定不是7.5NA, C不正确;D、乙酸是弱酸,存在电离平衡,所以1L 0.1mol/L乙酸溶液中H+数小于0.1NA,D不正确,答案选A。
考点:考查阿伏伽德罗常数的计算

练习册系列答案
相关题目
设NA代表阿伏加德罗常数的数值,下列说法中正确的是( )
| A.1.8 g重水(D2O)中含有的质子数和电子数均为1.0NA |
| B.0℃、1个标准大气压下,22.4L NO 和22.4L O2混合后所得气体中分子总数为1.5NA |
| C.含4mol Si-O键的二氧化硅晶体中,氧原子数为2NA |
| D.将11.2 L Cl2通入足量的石灰乳中制备漂白粉,转移的电子数为0.5NA |
0.5 molNa2SO4中含有Na+的数目是( )个。
| A.3.01×1023 | B.6.02×1023 | C.0.5 | D.1 |
用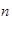 A表示阿伏加德罗常数的值。下列说法正确的是
A表示阿伏加德罗常数的值。下列说法正确的是
A.1 mol Cl-离子中含有的电子数为8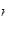 A A |
B.标准状况下,2.24 L H20中含有的分子数为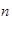 A A |
C.27g铝与足量的氧气反应,转移的电子数为3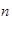 A A |
D.0.2 mo1·L-1 Ca(NO3)2溶液中含有的N03-离子数为0.4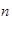 A A |
下列叙述中正确的是
| A.氧化还原反应中得失电子总数一定相等 |
| B.化学反应前后原子的总数一定不变 |
| C.电解质溶液中阴阳离子的总数一定相等 |
| D.分解反应一定是氧化还原反应 |
设NA为阿伏加德罗常数,下列叙述正确的是
| A.18g水中所含的电子数为8NA |
| B.11.2L氯气所含的分子数为0.5NA |
| C.2.4gMg与足量的盐酸反应失去的电子数为0.2NA |
| D.32g氧气中所含的氧原子数为NA |
下列化学用语正确的是
A.HClO的电子式: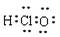 |
B.中子数为10的氧原子: |
C.硝基苯的结构简式: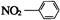 |
D.CH4分子的球棍模型: |
有Na2CO3、NaHCO3、CaO和NaOH组成的混合物28.2g,把它们溶于足量的水,充分反应后,溶液中Ca2+、CO32—、HCO3—均转化为沉淀,将容器中的水分蒸干,最后得到白色固体物质共30g。则下列有关叙述错误的是
| A.原混合物中含Na2CO3 0.1 mol |
| B.原混合物中n(Na2CO3)+n(NaHCO3)=n(CaO) |
| C.30g固体中一定存在n(CaCO3)<n(NaOH) |
| D.不能确定原混合物中NaOH的质量 |
下列化学用语的书写正确的是
| A.乙酸的分子式:C2H4O2 |
| B.乙醇的结构简式:C2H6O |
C.F原子结构示意图: |
D.四氯化碳的电子式: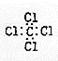 |