题目内容
【题目】工业碳酸钠(纯度约为98%)中含有Mg2+、Fe2+、Cl-和SO42-等杂质,提纯工艺流程如下。已知Fe2+在加热条件下易被氧气氧化为Fe3+,则下列说法错误的是
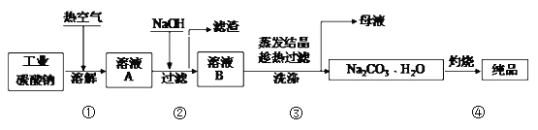
A. 步骤①,通入热空气可加快溶解速率
B. 步骤②,产生的滤渣的主要成分是Mg(OH)2和Fe(OH)2
C. 步骤③,趁热过滤后所得母液中含有Cl-、SO42-等离子
D. 步骤④,灼烧时用到的主要仪器有坩埚、泥三角、三脚架、酒精灯
【答案】B
【解析】
碳酸钠中混有Mg2+、Fe2+、Cl-和SO42-等杂质,在溶解时通入热空气可加快溶解速率、促进Fe2+的氧化,加入氢氧化钠,过滤后所得滤渣为氢氧化铁和氢氧化镁,溶液中主要含有碳酸钠,并含有少量的Cl-和SO42-,经蒸发结晶可得碳酸钠晶体,灼烧后可得碳酸钠,据此解答。
A. 步骤①是溶解,因此通入热空气可加快溶解速率,A正确;
B. 亚铁离子易被氧化为铁离子,则步骤②中产生的滤渣的主要成分是Mg(OH)2和Fe(OH)3,B错误;
C. 由于产生的滤渣中含有氢氧化铁和氢氧化镁,则步骤③,趁热过滤后所得母液中含有Cl-、SO42-等离子,C正确;
D. 步骤④是固体灼烧,灼烧时用到的主要仪器有坩埚、泥三角、三脚架、酒精灯,D正确。
答案选B。

练习册系列答案
相关题目



