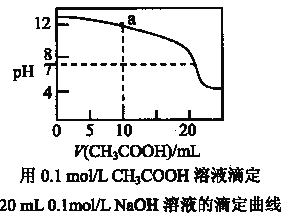
��Ŀ����
����Ŀ����֪ij��Һ��ֻ����OH-��H+��Na+��CH3COO-�������ӣ�ijͬѧ�Ʋ�������Ũ�ȴ�С˳�����������ֹ�ϵ��
��![]()
��![]()
��![]()
��![]()
��д���пհף�
��1������Һ���ܽ���һ�����ʣ����������______________�������Һ����������Ũ�ȵĴ�С˳���������4�ֹ�ϵ�е�______________��������ţ�
��2����������ϵ������ȷ�ģ�����Һ�е�����Ϊ______________����������ϵ������ȷ�ģ�����Һ�е�����Ϊ______________��
��3��������Һ���������ȵ�NaOH��Һ�ʹ����϶��ɣ���ǡ�ó����ԣ�����ǰc(NaOH)______c(CH3COOH)���>����<����=����ͬ������Ϻ���Һ��c(CH3COO-)______c(Na+)��
���𰸡� ![]() ��
�� ![]()
![]() < =
< =
����������1�����κ�ˮ��Һ�ж���OH-��H+��������ֻ��һ����ΪCH3COONa�����������ˮ����Һ�Լ��ԣ���c��H+����c��OH-������ˮ��ij̶Ⱥ�������c��Na+����c(CH3COO��)��c��OH������c��H+�������۷��ϣ���2�����е����ӹ�ϵ��֪��Һ�����ԣ���c(CH3COO��)��c��Na+����c��H+��������ҺΪ����������ƵĻ����Һ�����е����ӹ�ϵ��֪��Һ�Լ��ԣ���c��Na+����c��OH-����c(CH3COO��)������ҺΪ��������������ƵĻ����Һ����3���������Ũ����ͬ��NaOH��Һ�ʹ����ϣ���Һ�е�����Ϊ�����ƣ���Һ�Լ��ԣ�������Һǡ�ó����ԣ���ӦΪ����������ƵĻ����Һ������ǰc(NaOH)��c(CH3COOH)�����ݵ���غ��֪��Ϻ���Һ��c(CH3COO-)��c(Na+)��