题目内容
甲烷是天然气的主要成分,是生产生活中应用非常广泛的一种化学物质。
(1)一定条件下,用甲烷可以消除氮氧化物(NOx)的污染。已知:
①CH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g); △H1
②CH4(g) + 4NO2(g) =" 4NO(g)" + CO2(g) + 2H2O(g);△H2
现有一份在相同条件下对H2的相对密度为17的NO与NO2的混合气体,用16g甲烷气体催化还原该混合气体,恰好生成氮气、二氧化碳气体和水蒸气,共放出1042.8kJ热量。
①该混合气体中NO和NO2的物质的量之比为
②已知上述热化学方程式中△H1=—1160kJ/mol,则△H2=
③在一定条件下NO气体可以分解为NO2气体和N2气体,写出该反应的热化学方程式 。
(2)以甲烷为燃料的新型电池,其成本大大低于以氢为燃料的传统燃料电池,目前得到广泛的研究,下图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:

④B极为电池 极,电极反应式为
⑤若用该燃料电池做电源,用石墨做电极电解100mL 1mol/L的硫酸铜溶液,写出阳极的电极反应式 ,当两极收集到的气体体积相等时,理论上消耗的甲烷的体积为 (标况下),实际上消耗的甲烷体积(折算到标况)比理论上大,可能原因为 .
(1)一定条件下,用甲烷可以消除氮氧化物(NOx)的污染。已知:
①CH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g); △H1
②CH4(g) + 4NO2(g) =" 4NO(g)" + CO2(g) + 2H2O(g);△H2
现有一份在相同条件下对H2的相对密度为17的NO与NO2的混合气体,用16g甲烷气体催化还原该混合气体,恰好生成氮气、二氧化碳气体和水蒸气,共放出1042.8kJ热量。
①该混合气体中NO和NO2的物质的量之比为
②已知上述热化学方程式中△H1=—1160kJ/mol,则△H2=
③在一定条件下NO气体可以分解为NO2气体和N2气体,写出该反应的热化学方程式 。
(2)以甲烷为燃料的新型电池,其成本大大低于以氢为燃料的传统燃料电池,目前得到广泛的研究,下图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:

④B极为电池 极,电极反应式为
⑤若用该燃料电池做电源,用石墨做电极电解100mL 1mol/L的硫酸铜溶液,写出阳极的电极反应式 ,当两极收集到的气体体积相等时,理论上消耗的甲烷的体积为 (标况下),实际上消耗的甲烷体积(折算到标况)比理论上大,可能原因为 .
(1)①3:1 ②—574 kJ/mol ③4NO(g)=2NO2(g)+N2(g);△H=-293KJ/mol(2)④ 负CH4 + 4O2— —8e—= CO2+ 2H2O; ⑤4OH— —4e—= O2↑+ 2H2O 1.12L
甲烷不完全被氧化,生成C或CO 或 电池能量转化率达不到100%
甲烷不完全被氧化,生成C或CO 或 电池能量转化率达不到100%
试题分析:①设混合气体中NO和NO2的物质的量分别为X 、Y则(28X+46Y) ÷(X+Y)=2×17.解得X:Y=3:1.发生(①+②)÷2得③式:CH4(g)+2NO2(g)=N2(g)+CO2(g)+H2O(g) △H3=(△H1+△H2) ÷2.假设发生①的甲烷的物质的量为m;发生③的甲烷的物质的量为n. 则m+n=1;4m÷2n=3联立求解。解得m=0.6.n=0.4.0.4×{(△H1+△H2) ÷2} +0.6×△H1=-1042.8KJ/mol.将△H1=-1160KJ/mol代人该等式中,解得△H2=—574 kJ/mol.③△H3=(△H1+△H2) ÷2=-(1160 +574) kJ/mol÷2=-867KJ/mol. ①-③得④式:4NO(g) =2NO2(g)+N2(g) △H4=△H1-△H3=△H1-(△H1+△H2) ÷2=(△H1-△H2) ÷2=-293KJ/mol. 即NO气体可以分解为NO2气体和N2气的热化学方程式为:4NO(g)=2NO2(g)+N2(g);△H=-293KJ/mol。(2)④通入燃料甲烷的电极是负极,通入氧气的电极是正极。负极发生的电极式为CH4 + 4O2——8e—= CO2+ 2H2O ⑤电解硫酸铜溶液时阳极的电极反应式4OH— —4e—= O2↑+ 2H2O,阴极的反应式是: Cu2++2e-=Cu;2H++e-=H2↑。N(Cu)=0.1mol.若两极收集到的气体体积相等,设其物质的量为X。则4X=0.1×2+2X。解得X=0.1.在整个反应过程转移电子相等。电子的物质的量为0.4mol.由于没摩尔甲烷失去电子8摩尔,所以需要甲烷的物质的量为0.05摩尔。V(CH4)=0.05摩尔×22.4升/摩尔=1.12 升 。实际上消耗的甲烷体积比理论上大,可能原因是甲烷不完全被氧化,生成C或CO 或 电池能量转化率达不到100%。

练习册系列答案
相关题目
 O2(g)=H2 O(g) △H=-241.8kJ·mol-1
O2(g)=H2 O(g) △H=-241.8kJ·mol-1 2NO(g) △H
2NO(g) △H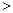 0,若1.0 mol空气含0.80 mol N2和0.20 mol O2,1300oC时在1.0 L密闭容器内经过5s反应达到平衡,测得NO为8.0×10-4 mol。
0,若1.0 mol空气含0.80 mol N2和0.20 mol O2,1300oC时在1.0 L密闭容器内经过5s反应达到平衡,测得NO为8.0×10-4 mol。 2CO2(g)+N2(g) 中,NO的浓度
2CO2(g)+N2(g) 中,NO的浓度
 H1=" +1175.7" kJ·mol-1
H1=" +1175.7" kJ·mol-1 H3=" +482.2" kJ·mol-1
H3=" +482.2" kJ·mol-1


 O2(g)=CO(g) ΔH2
O2(g)=CO(g) ΔH2 C(s)=
C(s)= CH3OH(g);ΔH=-90.8kJ·mol
CH3OH(g);ΔH=-90.8kJ·mol
 H2(g)+CO2(g),该反应平衡常数随温度的变化如下表所示:
H2(g)+CO2(g),该反应平衡常数随温度的变化如下表所示:
 CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。现在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下。下列说法正确的是
CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。现在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下。下列说法正确的是
 N2(g)+CO2(g)。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g)。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下: