题目内容
7.氨水呈弱碱性的原因是( )| A. | 通常状况下,氨气的溶解度较大 | |
| B. | 氨水中的NH3•H2O电离出少量的OH- | |
| C. | 溶于水的氨气生成的少量NH3•H2O全部电离生成OH- | |
| D. | 氨气本身的碱性弱 |
分析 一水合氨电离出氢氧根离子而使其溶液呈碱性,据此分析.
解答 解:氨气和水反应生成一水合氨,一水合氨电离出氢氧根离子而使溶液中氢氧根离子浓度大于氢离子浓度,则溶液呈碱性,电离方程式为:NH3•H2O?NH4++OH-,
故选B.
点评 本题考查了弱碱显碱性的原因,注意从其电离的角度分析,氢离子浓度与氢氧根离子浓度的相对大小决定溶液酸碱性,题目难度不大.

练习册系列答案
相关题目
17.石材的放射性常用镭(${\;}_{88}^{226}$Ra)作为标准,居里夫人(Marie Curie)因对Ra元素的研究曾两度获得诺贝尔奖.下列有关镭(${\;}_{88}^{226}$Ra)的叙述中不正确的是( )
| A. | ${\;}_{88}^{226}$Ra原子核内有138个中子 | B. | ${\;}_{88}^{226}$Ra原子核外有88个电子 | ||
| C. | ${\;}_{88}^{226}$Ra原子核内有88个质子 | D. | Ra元素位于第六周期 |
18.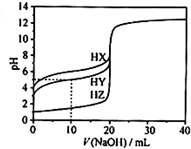 25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法不正确的是( )
25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法不正确的是( )
 25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法不正确的是( )
25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法不正确的是( )| A. | 在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ>HY>HX | |
| B. | 根据滴定曲线,可得Ka(HY)≈10-5 | |
| C. | 将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(Y-)>c(X-)>c(OH-)>c(H+) | |
| D. | HY与HZ混合,达到平衡时:c(H+)=$\frac{{k}_{2}(HY)•c(HY)}{c({Y}^{-})}$+c(Z-)+c(OH-) |
15.下列叙述中正确的是( )
| A. | 钠与硫酸铜溶液反应会置换出红色的铜 | |
| B. | 常温下干燥氯气与铁不反应,可以用钢瓶储存液氯 | |
| C. | CO2、NO2、SO2都能与H2O反应,其反应原理相同 | |
| D. | C、N、S三种单质直接与O2反应都能生成两种氧化物 |
2.在标准状况下,mgA气体与ngB气体分子数相等,下列说法不正确的是( )
| A. | 标准状况下,同体积的气体A、B质量比m:n | |
| B. | 25℃时,1Kg气体A与1Kg气体B的分子数之比为n:m | |
| C. | 同温同压下,气体A与气体B的密度之比为n:m | |
| D. | 标准状况下,等质量的A与B的体积比为n:m |
19.下列叙述中正确的是( )
| A. | 发生化学反应时,失去电子越多的金属原子,其还原能力越强 | |
| B. | 目前已发现118种元素,即已发现118种原子 | |
| C. | 核外电子总数相同的粒子,必定是同种元素的原子 | |
| D. | 同一元素的各种同位素的化学性质基本相同 |
16.分子式为C4H10O的醇与C5H10O2的羧酸和浓H2SO4存在时共热生成的酯有( )
| A. | 4种 | B. | 8种 | C. | 12种 | D. | 16种 |
17.化学与生活、社会密切相关,下列说法正确的是( )
| A. | 食品添加剂对人体的健康均无害,所以不用严格控制用量 | |
| B. | 棉、麻、丝、毛的主要成分都是纤维素 | |
| C. | 光纤的主要成分是二氧化硅 | |
| D. | 农业施肥所用的碳铵和尿素均属于无机物 |
