题目内容
1.在空气中,有下列反应发生:①N2+O2═2NO;②2NO+O2═2NO2;③3NO2+H2O═2HNO3+NO;④2SO2+O2═2SO3;⑤SO3+H2O═H2SO4;⑥SO2+H2O═H2SO3;⑦3O2═2O3.其中属于氧化还原反应的是( )| A. | ①②③④ | B. | ①②③④⑦ | C. | ①②④⑦ | D. | ①②③④⑤⑥⑦ |
分析 氧化还原反应的特征是元素化合价的变化,如发生氧化还原反应,则一定存在元素化合价的变化,结合具体的反应进行判断.
解答 解:①N和O元素化合价变化,属于氧化还原反应,故正确;
②N和O元素化合价变化,属于氧化还原反应,故正确;
③N元素化合价变化,由+4价分别变化为+5价和+2价,属于氧化还原反应,故正确;
④S和O元素化合价发生变化,属于氧化还原反应,故正确;
⑤元素化合价没有发生变化,不是氧化还原反应,故错误;
⑥元素化合价没有发生变化,不是氧化还原反应,故错误;
⑦元素化合价没有发生变化,不是氧化还原反应,故错误.
故选A.
点评 本题考查氧化还原反应,为高频考点,侧重于学生的分析能力和基本概念的理解和运用的考查,注意从元素化合价的角度认识氧化还原反应的相关概念和物质的性质,难度不大.

练习册系列答案
相关题目
9.下列说法正确的是( )
| A. | 146C的中子数为14 | B. | 146C的质子数为14 | ||
| C. | 146C和126C互为同位素 | D. | 146C的摩尔质量为14 |
16.在粗盐提纯实验中,要溶解10g粗盐,所需要量取水的体积最佳为(常温下氯化钠的溶解度为36g/100g水)( )
| A. | 100mL | B. | 40mL | C. | 50mL | D. | 30mL |
6.决定气体体积的主要因素是( )
①微粒的大小 ②微粒的数目 ③微粒之间的距离.
①微粒的大小 ②微粒的数目 ③微粒之间的距离.
| A. | ①② | B. | ①③ | C. | ②③ | D. | ①②③ |
13.工业上用CO生产甲醇的反应为CO(g)+2H2(g)?CH3OH(g).图1表示反应中能量的变化;图2表示一定温度下,在体积固定为2L的密闭容器中加入4mol H2和一定量的CO(g)后,CO(g)和CH3OH(g)的浓度随时间的变化图.下列叙述错误的是( )
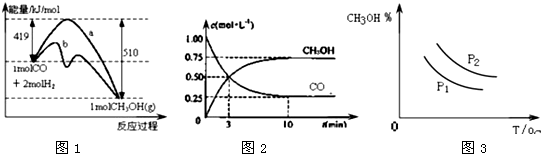

| A. | CO和H2合成CH3OH的反应:△H<0,△S<0 | |
| B. | 保持温度不变,再充入1molCO和2molH2,反应达到新平衡时$\frac{n(CHOH)}{n(CO)}$减小 | |
| C. | 图1中曲线b可表示使用了催化剂的能量变化情况 | |
| D. | 图3中曲线可表示在不同压强P1、P2(P1<P2)条件下甲醇百分含量随温度变化的情况 |
10.下列说法或表示方法正确的是( )
| A. | 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 | |
| B. | 由H+(aq)+OH-(aq)=H2O(I);△H=-57.3kJ•mol-1molCH3COOH的稀溶液与含l mol NaOH的稀溶液混合,放出的热量小于57.3 kJ | |
| C. | 由C(石墨)=(金刚石);△H=+1.90kJ•mol-1可知,金刚石比石墨稳定 | |
| D. | 500℃、30MPa下,将0.5 mol(g)和1.5 mol (g)置于密闭容器中充分反应生成(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g);△H=-38.6kJ•mol-1 |
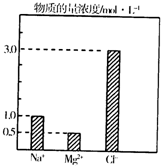 金属及其化合物有广泛的应用.
金属及其化合物有广泛的应用.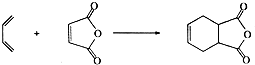
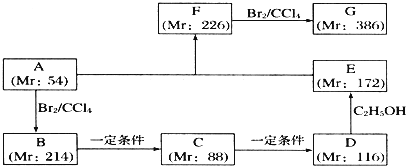
 .
.