题目内容
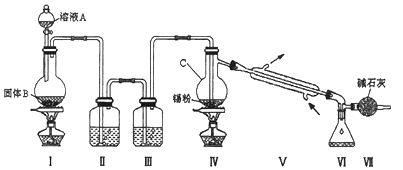
【题目】将物质的量均为3.00mol物质A,B混合于5L容器中,发生如下反应:3A+B2C,在反应过程中C的物质的量分数随温度变化如图所示: 
(1)T0对应的反应速率v(正)v(逆)(用“=”、“>”或“<”表示,下同);
(2)此反应的正反应为热;(填“放”或“吸”)
(3)X,Y两点A物质正反应速率的大小关系是YX;
(4)温度T<T0时,C%逐渐增大的原因是:;
(5)若Y点的C的物质的量分数为25%,则参加反应的A物质的量为mol.
【答案】
(1)=
(2)放
(3)>
(4)反应未达平衡,仍在向正反应方向移
(5)1.8
【解析】解:(1)起始时加入物质的量均为3.00mol的物质A、B,随着温度的升高,反应向正反应方向进行,当温度达到T0时,C的物质的量分数最大,说明达到反应的最大限度,即平衡状态,此时正逆反应速率相等,故答案为:=(2)随着温度的继续升高,C的物质的量分数逐渐减小,说明温度升高平衡左移,则正反应为放热反应,故答案为:放;(3)温度越高,反应速率越大,Y点温度大于X点,则X点反应速率小于Y点,故答案为:Y>X(4)温度T0前,反应还没有到达平衡,反应向正反应进行,随着温度升高,生成的C越来越多,故答案为:反应还没有到达平衡,反应向正反应进行;(5)设参加反应的A的物质的量为x,根据方程式知:平衡状态时A的物质的量=(3﹣x)mol,B的物质的量=(3﹣ ![]() )mol,C的物质的量=
)mol,C的物质的量= ![]() xmol,C的物质的量分数=
xmol,C的物质的量分数=  ×100%=25%,x=1.8mol,
×100%=25%,x=1.8mol,
故答案为:1.8.
(1)起始时加入物质的量均为3.00mol的物质A、B,随着温度的升高,反应向正反应方向进行,当温度达到T0时,C的物质的量分数最大,说明达到反应的最大限度,即平衡状态,此时正逆反应速率相等;(2)随着温度的继续升高,C的物质的量分数逐渐减小,说明温度升高平衡左移;(3)温度越高,反应速率越大;(4)反应还没有到达平衡,反应正向进行,随着温度升高,生成的C越来越多;(5)设参加反应的A的物质的量为x,根据方程式知:平衡状态时A的物质的量=(3﹣x)mol,B的物质的量=(3﹣ ![]() )mol,C的物质的量=
)mol,C的物质的量= ![]() xmol,C的物质的量分数=
xmol,C的物质的量分数=  ×100%=25%,从而计算参加反应的A的物质的量.
×100%=25%,从而计算参加反应的A的物质的量.

 计算高手系列答案
计算高手系列答案