题目内容

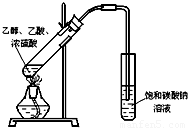
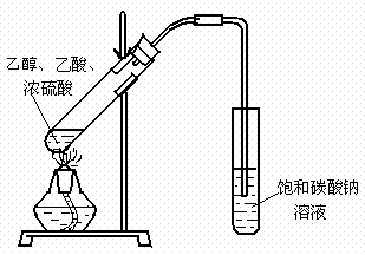
 (1)某实验小组用右图装置制取乙酸乙酯,请回答下列问题:
(1)某实验小组用右图装置制取乙酸乙酯,请回答下列问题:①该装置有一处错误,请指出错误
导管伸入碳酸钠溶液液面下
导管伸入碳酸钠溶液液面下
;并说出该错误可能引起的后果是
可能发生倒吸
可能发生倒吸
.②能证明该实验有新物质(乙酸乙酯)生成最明显和直接的现象是
饱和碳酸钠溶液液面上出现一层无色油状液体
饱和碳酸钠溶液液面上出现一层无色油状液体
.③完成该反应的化学方程式
CH3CH218OH+CH3COOH
CH3CH218OH+CH3COOH
| ||
| △ |
CH3CO18OCH2CH3+H2O
CH3CO18OCH2CH3+H2O
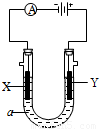
.(产物中标出18O的位置)(2)电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a,a是CuCl2溶液,X、Y都是石墨电极,通过导线与直流电源相连.

①X极是
阴
阴
极(填正、负、阴或阳),X极上现象析出红色固体
析出红色固体
②Y极上的电极反应式
2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
;③若反应过程中在Y极上产生气体224mL(标准状况),则此过程中电源需提供的电量是
1.204×1022Q
1.204×1022Q
.(已知每个电子带的电量为Q,用含Q的式子表示)分析:(1)①反应试管受热不均,盛饱和碳酸钠溶液的试管中的导管伸入液面下可能发生倒吸;
②乙醇与乙酸都能溶于水,乙酸乙酯不溶于水,溶液分层,密度比水小,乙酸乙酯在上层;
③羧酸与醇发生的酯化反应中,羧酸中的羧基提供-OH,醇中的-OH提供-H,相互结合生成水,剩余基团结合生成乙酸乙酯;
(2)①电解池连接电源负极的电极是阴极,阴极放出还原反应,阳离子在阴极放电,溶液中Cu2+氧化性最强,故Cu2+放电
生成Cu;
②Y极连接电源的正极,是电解池的阳极,发生氧化反应,Cl-在阳极放电生成Cl2;
③极上产生224mL气体是氯气,计算氯气的物质的量,根据电子转移计算转移的电子的物质的量,进而计算电源需提供的电量.
②乙醇与乙酸都能溶于水,乙酸乙酯不溶于水,溶液分层,密度比水小,乙酸乙酯在上层;
③羧酸与醇发生的酯化反应中,羧酸中的羧基提供-OH,醇中的-OH提供-H,相互结合生成水,剩余基团结合生成乙酸乙酯;
(2)①电解池连接电源负极的电极是阴极,阴极放出还原反应,阳离子在阴极放电,溶液中Cu2+氧化性最强,故Cu2+放电
生成Cu;
②Y极连接电源的正极,是电解池的阳极,发生氧化反应,Cl-在阳极放电生成Cl2;
③极上产生224mL气体是氯气,计算氯气的物质的量,根据电子转移计算转移的电子的物质的量,进而计算电源需提供的电量.
解答:解:(1)①反应试管受热不均,盛饱和碳酸钠溶液的试管中的导管伸入液面下可能发生倒吸;
故答案为:导管伸入碳酸钠溶液液面下;可能发生倒吸;
②乙醇与乙酸都能溶于水,乙酸乙酯不溶于水,溶液分层,密度比水小,乙酸乙酯在上层,饱和碳酸钠溶液液面上出现一层无色油状液体,说明有新物质生成;
故答案为:饱和碳酸钠溶液液面上出现一层无色油状液体;
③羧酸与醇发生的酯化反应中,羧酸中的羧基提供-OH,醇中的-OH提供-H,相互结合生成水,剩余基团结合生成乙酸乙酯,同时该反应可逆,反应的化学方程式为CH3CH218OH+CH3COOH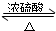 CH3CO18OCH2CH3+H2O;
CH3CO18OCH2CH3+H2O;
故答案为:CH3CH218OH+CH3COOH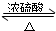 CH3CO18OCH2CH3+H2O;
CH3CO18OCH2CH3+H2O;
(2)①电解池连接电源负极的电极是阴极,阴极放出还原反应,阳离子在阴极放电,溶液中Cu2+氧化性最强,故Cu2+放电
发生反应Cu2++2e-=Cu↑,X极上现象析出红色固体;
故答案为:阴,析出红色固体;
②Y极连接电源的正极,是电解池的阳极,发生氧化反应,Cl-在阳极放电生成Cl2,电极反应式为2Cl--2e-=Cl2↑;
故答案为:2Cl--2e-=Cl2↑;
③极上产生224mL气体是氯气,氯气的物质的量为
=0.01mol,根据电子转移守恒可知转移的电子的物质的量为0.01mol×2=0.02mol,故电源需提供的电量为0.02mol×6.02×1023mol-1×Q=1.204×1022Q;
故答案为:1.204×1022Q.
故答案为:导管伸入碳酸钠溶液液面下;可能发生倒吸;
②乙醇与乙酸都能溶于水,乙酸乙酯不溶于水,溶液分层,密度比水小,乙酸乙酯在上层,饱和碳酸钠溶液液面上出现一层无色油状液体,说明有新物质生成;
故答案为:饱和碳酸钠溶液液面上出现一层无色油状液体;
③羧酸与醇发生的酯化反应中,羧酸中的羧基提供-OH,醇中的-OH提供-H,相互结合生成水,剩余基团结合生成乙酸乙酯,同时该反应可逆,反应的化学方程式为CH3CH218OH+CH3COOH
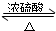 CH3CO18OCH2CH3+H2O;
CH3CO18OCH2CH3+H2O;故答案为:CH3CH218OH+CH3COOH
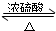 CH3CO18OCH2CH3+H2O;
CH3CO18OCH2CH3+H2O;(2)①电解池连接电源负极的电极是阴极,阴极放出还原反应,阳离子在阴极放电,溶液中Cu2+氧化性最强,故Cu2+放电
发生反应Cu2++2e-=Cu↑,X极上现象析出红色固体;
故答案为:阴,析出红色固体;
②Y极连接电源的正极,是电解池的阳极,发生氧化反应,Cl-在阳极放电生成Cl2,电极反应式为2Cl--2e-=Cl2↑;
故答案为:2Cl--2e-=Cl2↑;
③极上产生224mL气体是氯气,氯气的物质的量为
| 0.224L |
| 22.4L/mol |
故答案为:1.204×1022Q.
点评:本题考查乙酸乙酯的制备、电解池工作原理等,难度不大,注意乙酸乙酯实验混合液的配制、饱和碳酸钠溶液的作用以及酯化反应的机理.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
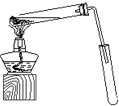 某化学实验小组用右图所示的装置制取乙酸乙酯,并检验乙 酸 乙 酯中是否含有乙酸杂质(铁架台、夹子等支撑仪器省略).已知乙酸乙酯的沸点为77.1℃,乙醇沸点为78.4℃,乙酸的沸点为118℃.请根据要求填空:
某化学实验小组用右图所示的装置制取乙酸乙酯,并检验乙 酸 乙 酯中是否含有乙酸杂质(铁架台、夹子等支撑仪器省略).已知乙酸乙酯的沸点为77.1℃,乙醇沸点为78.4℃,乙酸的沸点为118℃.请根据要求填空: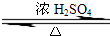 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O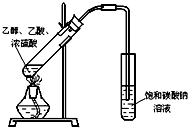
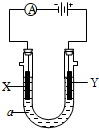
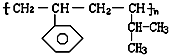
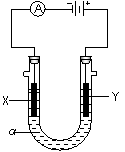 (2)电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a,a是CuCl2溶液,X、Y都是石墨电极,通过导线与直流电源相连。
(2)电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a,a是CuCl2溶液,X、Y都是石墨电极,通过导线与直流电源相连。 .(产物中标出18O的位置)
.(产物中标出18O的位置)