题目内容
【题目】氮和氮的化合物在工农业生产、国防和生活中都有极其广泛的用途。请回答下列与氮元素有关的问题:
(1)亚硝酸氯(结构式为Cl-N=O)是有机合成中的重要试剂,可由Cl2和NO在通常条件下反应制得,反应方程式为![]() 。
。
已知几种化学键的键能数据如表所示:
化学键 |
|
|
|
|
键能( | 243 | a | 607 | 630 |
当Cl2与NO反应生成ClNO的过程中转移了4mol电子,理论上放出的热量为___kJ。(用数字和字母表示)
(2)温度一定时,在一个体积为1L的密闭容器中通入2mol NO和1mol Cl2,10min时ClNO体积占气体总体积40%,反应开始到10min内NO的平均反应速率:![]() =___
=___![]() 。
。
(3)利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,装置如图所示:
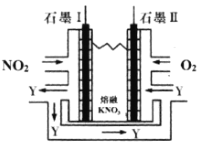
电池工作时,NO2转变成绿色硝化剂Y(N2O5),可循环使用,则石墨Ⅱ为电源____极,石墨Ⅱ附近发生的电极反应式为___。
(4)含氮废水进入水体会造成富营养化,常使用次氯酸去除氨氮(以NH4+表示),生成无毒无害物质。次氯酸氧化除去氨氮的离子反应方程式是____。
【答案】![]() 0.1 正
0.1 正 ![]()
![]()
【解析】
(1)先依据所给的化学方程式找到转移电子数与放热的关系,然后列正比例式进行求算;
(2)利用三段式求出NO的浓度改变量,除以时间即可;
(3)明确价态变化,明确正负极,考虑题给信息,写出电极反应式;
(4)根据题给的信息,明确反应物和产物,利用化合价升降总数相等配平即可。
(1)从反应方程式2NO+Cl2![]() 2ClNO来看,每消耗1mol Cl2,转移2mol电子,放出的热量为(a+607)×2-2×630-243=(2a-289)kJ,所以转移4mol电子,放出热量为2×(2a-289)kJ=(4a-578)kJ;
2ClNO来看,每消耗1mol Cl2,转移2mol电子,放出的热量为(a+607)×2-2×630-243=(2a-289)kJ,所以转移4mol电子,放出热量为2×(2a-289)kJ=(4a-578)kJ;
(2) 根据化学方程式:
2NO(g)+Cl2(g)![]() 2ClNO(g)
2ClNO(g)
初始 2 1 0
变化 2x x 2x
剩余 2-2x 1-x 2x
10min时ClNO体积占气体总体积的40%,则其物质的量分数也为40%,即![]() =0.4,解得x=0.5mol,所以开始到10min内NO的平均反应速率
=0.4,解得x=0.5mol,所以开始到10min内NO的平均反应速率![]() =0.1mol·L-1·min-1;
=0.1mol·L-1·min-1;
(3)石墨II处通入了O2,发生了还原反应,对应原电池的正极。发生的电极反应式为:O2+N2O5+4e-=2NO3-,注意看清图示中的N2O5进入了正极区域;
(4)次氯酸是强氧化剂,NH4+被氧化为氮气,反应的离子方程式为:2NH4++3HClO=N2↑+3H2O+5H++3Cl-。