题目内容
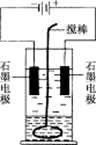
常温下用石墨电极,电解100 mL 0.1 mol·L-1 Cu(NO3)2和0.1 mol·L-1 AgNO3组成的混合溶液,当某一电极上生成的气体在标准状况下体积为1.12 L时,假设溶液体积不变,下列说法正确的是
| A.阴极增重1.72 g | B.所得溶液 pH<1 |
| C.阴极增重0.64 g | D.所得溶液pH>1 |
AB
溶液中铜离子和银离子的物质的量都是0.01mol,根据放电顺序可知,阴极首先是银离子放电,生成银,然后是铜离子放电生成铜。阳极是OH-放电生成氧气,即氧气是0.05mol,转移电子是0.2mol,所以根据电子的得失守恒可知,阴极除了生成0.01mol银和铜外,还生成0.085mol氢气,所以阴极增加的质量是1.08g+0.64g=1.72g,A正确;在金属离子放电的同时,溶液中产生氢离子,所以B也正确,答案选AB。

练习册系列答案
相关题目
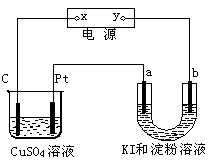
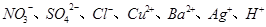 中选出适当离子组成的电解质(非熔融态下),并电解,
中选出适当离子组成的电解质(非熔融态下),并电解,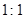 ,电解质所有可能为 。
,电解质所有可能为 。