题目内容
化合物AX3和单质X2在一定条件下反应可生成化合物AX5。回答下列问题:
(1)反应AX3(g)+X2(g) AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。

① 图中3组实验从反应开始至达到平衡时的反应速率v(AX5)由大到小的次序为 (填实验序号);与实验a相比,其他两组改变的实验条件及判断依据是:b 、c 。
②用p0表示开始时总压强,p表示平衡时总压强,α表示AX3的平衡转化率,则α的表达式为 ;实验a平衡转化率:α(a)为 。
(2)已知AX3的熔点和沸点分别为-93.6 ℃和76 ℃,AX5的熔点为167 ℃。室温时AX3与气体X2反应生成lmol AX5,放出热量123.8 kJ。该反应的热化学 方程式为 。
方程式为 。
 阅读快车系列答案
阅读快车系列答案有A、B、C、D四种强电解质,它们在水中电离产生下列离子(每种物质只含一种阴离子且互不重复)。
阳离子 | Na+、Ba2+、NH |
阴离子 | CH3COO-、OH-、Cl-、SO |
已知:①A、C溶液的pH均大于7,A、B的溶液中水的电离程度相同;②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无现象。
(1)A是_____________,B是____________(填化学式) 。用离子方程式表示A的水溶液中存在的平衡关系: 。
(2)25 ℃时,0.1 mol ·L-1 B溶液的pH=a,则B溶液中:c(H+)-c(OH—)=_____________(填微粒浓度符号)=_____________(用含有a的关系式表示)。
·L-1 B溶液的pH=a,则B溶液中:c(H+)-c(OH—)=_____________(填微粒浓度符号)=_____________(用含有a的关系式表示)。
(3)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序是_____________。
(4)在一定体积的0.005 mol·L-1的C溶液中,加入一定体积的0.00125 mol·L-1的盐酸,混合溶液的pH=11,若反应后溶液的体积等于C溶液与盐酸的体积之和,则C溶液与盐酸的体积比是_ _____。
(5)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl?,利用Ag+与CrO42?生成砖红色沉淀,指示到达滴定终点。当溶液中Cl?恰好沉淀完全(浓度等于1.0×10?5 mol·L?1)时,溶液中c(Ag+)为_______ mol·L?1,此时溶液中c(CrO42?)等于__________ mol·L?1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10?12和2.0×10?10)。
(6)现使用酸碱中和滴定法测定酸的浓度。在本实验的滴定过程中,下列操作会使实验结果偏大的是 (填写序号)。
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测酸溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出


 CO2(g) + H2(g) △H<0,CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)= mol·L-1·min-1。
CO2(g) + H2(g) △H<0,CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)= mol·L-1·min-1。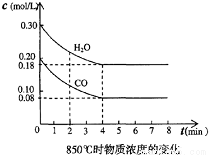





 OH-)>c(Na+)=c(NH3·H2O)
OH-)>c(Na+)=c(NH3·H2O) )+c(H+)=c(OH-)
)+c(H+)=c(OH-) )+c(Na+)
)+c(Na+) 中= 1×10-8,相同物质的量浓度的某一元碱(BO
中= 1×10-8,相同物质的量浓度的某一元碱(BO H)溶液中
H)溶液中
