题目内容
5.下面是对四个实验绘制的图形,其中实验结果与图形对应准确的是( )
| A. | 图①是pH=13的NaOH溶液中加水稀释 | |
| B. | 图②是用适量的KClO3和MnO2混合物加热制O2 | |
| C. | 图③是向一定量的稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量 | |
| D. | 图④向一定质量的稀盐酸中加入铁粉至过量 |
分析 A.PH=13属碱性溶液,加水稀释碱性减弱;
B.氯酸钾与二氧化锰混合加热时开始一段时间不会产生氧气;
C.稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液时,开始时盐酸与碳酸钠反应会生成气体,盐酸消耗,有沉淀生成;
D.铁和稀盐酸发应生成氢气,根据稀盐酸反应后不再产生氢气分析.
解答 解:A.PH=13属碱性溶液,加水稀释碱性减弱,对于碱性溶液来说,碱碱性越弱PH越小,但不管怎样稀释PH不可能小于7,故A错误.
B.氯酸钾与二氧化锰混合加热时开始一段时间不会产生氧气,加热一段时间后才会有氧气的放出,故B错误.
C.向一定量的稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量,盐酸与碳酸钠反应时是不会有沉淀生成的,故碳酸钠加入一会盐酸消耗掉才有沉淀,坐标图正确,故C正确;
D.一定质量的稀盐酸与铁反应,等稀盐酸反应后不再产生氢气,应该趋于水平,故D错误;
故选C.
点评 本题考查元素化合物的应用,侧重对物质的变化过程与图象结合题的考查,对反应过程的详细分析并结合图象走势是解题的关键,题目难度中等.

练习册系列答案
 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
9.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 相同质量的N2和CO所含有的分子数、原子总数、电子总数都相等 | |
| B. | 50ml18.4 mol/L浓硫酸与足量铜加热反应,生成S02分子的数目为0.4 6 NA | |
| C. | 0.1mol/LMgCl2溶液中含有的Mg2+数目一定小于0.1NA | |
| D. | 1 mol CH5+中含有的电子数目为11NA |
10.氯碱工业是基础化学工业,在隔膜电解槽内电解氯化钠的饱和溶液可以得到H2,Cl2,NaOH,并由此形成氯碱产品系列.若将电解槽的内隔膜去掉,同时升高电解液的温度,此时电解产物间发生反应:Cl2+NaOH→NaClO3+NaCl+H2O (未配平),假设反应进行完全,则在该条件下最后得到的两种产物的物质的量之比是( )
| A. | 1:1 | B. | 1:2 | C. | 1:5 | D. | 2:3 |
20.化学实验中处处表现出颜色变化,下列化学实验在的颜色变化不符合实验事实的是( )
| A. | 铁钉放入硫酸铜溶液中,溶液由蓝色变为浅绿色 | |
| B. | 将空气中燃着的硫伸入氧气瓶中,火焰由黄色变为蓝紫色 | |
| C. | 高温加热木炭与氧化铜的混合物,固体由黑色变成红色 | |
| D. | 往水中加入少量高锰酸钾,液体由无色变成紫红色 |
14.X、Y、Z、Q、M为常见的短周期元素,其原子序数依次增大.有关信息如下表:
(1)X的气态氢化物的大量生产曾经解决了地球上因粮食不足而导致的饥饿和死亡问题,请写出该气态氢化物的电子式 .
.
(2)已知37Rb和53I都位于第五周期,分别与Z和M同一主族.下列有关说法正确的是ACD(填序号).
A.原子半径:Rb>I
B.RbM中含有共价键
C.气态氢化物热稳定性:M>I
D.Rb、Q、M的最高价氧化物对应的水化物可以两两发生反应
(3)若XM3最初水解产物是XH3和HMO,则X、M元素的电负性大小顺序是:X>M((填>、<、或=);若已知磷与M元素电负性关系是:P<M,则PM3水解的化学反应方程式是PCl3+3H2O=3HCl+H3PO3.
(4)X、Y组成的一种无色气体遇空气变为红棕色.将标准状况下40L该无色气体与15L氧气通入一定浓度的NaOH溶液中,恰好被完全吸收,同时生成两种盐.请写出该反应的离子方程式8NO+3O2+8OH-=2NO3-+6NO2-+4H2O.
| X | 动植物生长不可缺少的元素,是组成蛋白质的重要元素 |
| Y | 地壳中含量居第一位 |
| Z | 短周期中其原子半径最大 |
| Q | 生活中大量使用其合金制品,工业上可用电解其氧化物的方法制备 |
| M | 海水中大量富集的元素之一,其最高正化合价与负价的代数和为6 |
 .
.(2)已知37Rb和53I都位于第五周期,分别与Z和M同一主族.下列有关说法正确的是ACD(填序号).
A.原子半径:Rb>I
B.RbM中含有共价键
C.气态氢化物热稳定性:M>I
D.Rb、Q、M的最高价氧化物对应的水化物可以两两发生反应
(3)若XM3最初水解产物是XH3和HMO,则X、M元素的电负性大小顺序是:X>M((填>、<、或=);若已知磷与M元素电负性关系是:P<M,则PM3水解的化学反应方程式是PCl3+3H2O=3HCl+H3PO3.
(4)X、Y组成的一种无色气体遇空气变为红棕色.将标准状况下40L该无色气体与15L氧气通入一定浓度的NaOH溶液中,恰好被完全吸收,同时生成两种盐.请写出该反应的离子方程式8NO+3O2+8OH-=2NO3-+6NO2-+4H2O.
15.下列化合物中,既可看作醇,又可看作酚的是( )
| A. | 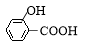 | B. | 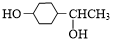 | C. | 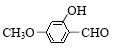 | D. | 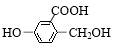 |
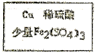 $→_{过滤}^{调节PH_{3}-4}$CuSO4溶液$→_{过滤}^{结晶}$CuSO4•5H2O
$→_{过滤}^{调节PH_{3}-4}$CuSO4溶液$→_{过滤}^{结晶}$CuSO4•5H2O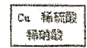 $\stackrel{40℃-50℃}{→}$CuSO4溶液$→_{过滤}^{结晶}$CuSO4•5H2O
$\stackrel{40℃-50℃}{→}$CuSO4溶液$→_{过滤}^{结晶}$CuSO4•5H2O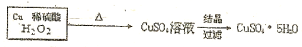 .
.