题目内容
15.下列反应的离子方程式正确的是( )| A. | 碳酸钙溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O | |
| B. | 苯酚钠溶液中通入少量的CO2:2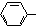 O-+CO2+H2O→2 O-+CO2+H2O→2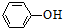 +CO32- +CO32- | |
| C. | 乙醛与新制的氢氧化铜悬浊液:CH3CHO+2Cu(OH)2+OH-$\stackrel{△}{→}$CH3COO-+Cu2O↓+3H2O | |
| D. | 氯乙酸与足量氢氧化钠溶液共热:ClCH2COOH+OH- $\stackrel{△}{→}$ ClCH2COO-+H2O |
分析 A.醋酸属于弱电解质,离子方程式中醋酸应该保留分子式;
B.苯酚的酸性大于碳酸氢根离子,二者反应生成碳酸氢钠和苯酚,不是生成碳酸钠;
C.乙醛分子中含有醛基,能够与新制的氢氧化铜浊液反应生成氧化亚铜沉淀;
D.在氢氧化钠的水溶液中,氯原子发生取代反应生成羟基.
解答 解:A.醋酸是弱酸要写成分子式的形式,正确的离子方程式为:CaCO3+2CH3COOH═2CH3COO-+Ca2++H2O+CO2↑,故A错误;
B.向苯酚钠溶液中通入少量的CO2,反应生成苯酚和碳酸氢钠,正确的离子反应为:C6H5O-+CO2+H2O→C6H5OH+HCO3-,故B错误;
C.乙醛与新制的氢氧化铜悬浊液发生氧化还原反应,反应的离子方程式为:CH3CHO+2Cu(OH)2+OH-$\stackrel{△}{→}$CH3COO-+Cu2O↓+3H2O,故C正确;
D.氯乙酸与足量氢氧化钠溶液共热,二者发生中和反应和取代反应(或水解反应)反应生成CH2(OH)COONa,正确的离子方程式为:ClCH2COOH+2OH- $\stackrel{△}{→}$ CH2(OH)COO-+H2O+Cl-,故D错误;
故选C.
点评 本题考查了离子方程式的书写判断,题目难度中等,明确发生反应实质及离子方程式的书写原则为解答关键,B为易错点,注意苯酚与少量二氧化碳反应生成的是碳酸氢钠.

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
5.0.1mol•L-1 AgNO3溶液在以Ag作阳极、Fe作阴极的电解槽中电解,当阴极上增重2.16g时,下列判断正确的是( )
| A. | 溶液的浓度变为0.08 mol•L-1 | B. | 阳极上产生112 mL O2(标准状况) | ||
| C. | 转移的电子数是1.204×1022 | D. | 反应中有0.02 mol的Ag被氧化 |
6.下列说法正确的是( )
| A. | 在粗硅的制取中发生反应2C+SiO2$\frac{\underline{\;高温\;}}{\;}$2CO↑+Si,所以非金属性C>Si | |
| B. | 由Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$CO2↑+Na2SiO3可知硅酸的酸性大于碳酸 | |
| C. | 用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后再通入CO2 | |
| D. | 由H2S+CuSO4═CuS↓+H2SO4可知,氢硫酸的酸性比硫酸强 |
3.下列说法不正确的是( )
| A. | 正常雨水的pH为7.0,酸雨的pH小于7.0 | |
| B. | 严格执行机动车尾气排放标准有利于防止大气污染 | |
| C. | 使用二氧化硫和某些含硫化合物漂白食品会对人体健康产生危害 | |
| D. | PM 2.5是指大气中直径≤2.5微米的颗粒物,戴普通口罩还是对人体健康有影响 |
7.已知R-X+2Na+R′-X→R-R′+2NaX,若用CH3CH2Br和 (CH3)2CHBr 的混合物与金属钠反应,生成的烷烃不可能是( )
| A. | CH3CH2CH2CH3 | B. | CH3CH2CH2CH2CH3 | C. | (CH3)2CHCH(CH3)2 | D. | CH3CH2CH(CH3)2 |
4.漂白粉的有效成分是( )
| A. | Ca(ClO)2 | B. | CaCl2 | C. | NaOH | D. | NaClO |
 .
.