题目内容
【题目】下列说法正确的是(用NA表示阿伏加德罗常数的值)
A. 17g羟基(-OH)所含有的电子数是10 NA个
B. 常温下,14g乙烯含有的共用电子对数是2.5NA个
C. 12 g石墨中含有C﹣C键的个数为1.5NA
D. 标准状况下,CH4发生取代反应生成22.4LCH2Cl2,需要消耗2NA个Cl2分子
【答案】C
【解析】
A、17g羟基(-OH)的物质的量为1mol,在一个羟基中含有9个电子,所以1mol的羟基中所含有的电子数是9 NA个,故A错误;
B、有机物中一个碳原子周围总有4个共用电子对,14g乙烯的物质的量为:![]() =0.5mol,则14g乙烯含有的共用电子对数是2NA个,故B错误;
=0.5mol,则14g乙烯含有的共用电子对数是2NA个,故B错误;
C、12 g石墨的物质的量n=![]() =1mol,石墨中每个C原子与其它3个C原子成键,则平均每个C原子成键数目为3
=1mol,石墨中每个C原子与其它3个C原子成键,则平均每个C原子成键数目为3![]() =1.5个,则12 g石墨含C﹣C键的个数为1.5NA,所以C选项是正确的;
=1.5个,则12 g石墨含C﹣C键的个数为1.5NA,所以C选项是正确的;
D、标准状况下,CH2Cl2为液态,22.4LCH2Cl2不是1mol,故D错误。
所以C选项是正确的。

【题目】利用铜萃取剂M,通过如下反应实现铜离子的富集:
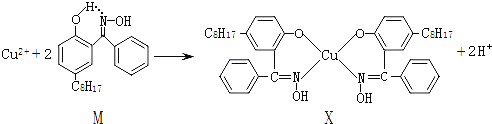
(1)关于M所含元素的说法正确的是______________。
A.电负性由大到小顺序:O>N>C>H
B.第一电离能由大到小的顺序:O>N>C
C.氮原子以sp2杂化轨道与氧原子形成σ键
D.从物质分类角度M属于芳香烃,M中所有的碳原子不可能共面
E.组成M元素的氢化物稳定性:CH4<H2O<NH3
(2)上述反应中断裂和生成的化学键有_______(填序号)。
A.氢键 B.配位键 C.金属键 D.范德华力 E.共价键 F.离子键
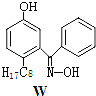
(3)M与W(分子结构如上图)相比,M的水溶性小,更利于Cu2+的萃取。M水溶性小的主要原因是_______________。
(4)基态Cu2+的外围电子排布图为________________,Cu2+等过渡元素水合离子是否有颜色与原子结构有关,且存在一定的规律。判断Sc3+、Zn2+的水合离子为无色的依据是_____________________________________________________________。
离子 | Sc3+ | Ti3+ | Fe2+ | Cu2+ | Zn2+ |
颜色 | 无色 | 紫红色 | 浅绿色 | 蓝色 | 无色 |
(5)已知:Y原子最高价氧化物对应水化物的酸性最强。铜与Y形成化合物的晶胞如附图所示(黑点代表铜原子,空心圆代表Y原子)。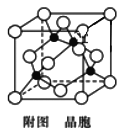
①该晶体的化学式为_______________。(用元素符号表示)
②已知铜和Y原子的电负性分别为1.9和3.0,则铜与Y原子形成的化合物属于____________(填“离子”或“共价”)化合物。
③已知该晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,则该晶体中铜原子与Y原子之间的最短距离为_______________pm(只写计算式)。