题目内容
(2013?房山区一模)下列解释实验现象的反应方程式正确的是( )
分析:离子方程式是指用实际参加反应的离子符号表示离子反应的式子.离子方程式的书写步骤一般为:
①“写”:写出有关反应的化学方程式;②“拆”:可溶性的电解质用离子符号表示,其它难溶的物质、气体、水等仍用化学式表示;③“删”:删去方程式两边不参加反应的离子; ④“查”:检查式子两边的各种原子的个数及电荷数是否相等;
A.乙酸根离子水解是可逆反应;
B.氯气的氧化性大于过氧化氢;
C.将相互接触的铜片和锌片置于稀硫酸中,构成原电池,锌为原电池的负极;
D.硫化铜的溶解度小于氢氧化铜.
①“写”:写出有关反应的化学方程式;②“拆”:可溶性的电解质用离子符号表示,其它难溶的物质、气体、水等仍用化学式表示;③“删”:删去方程式两边不参加反应的离子; ④“查”:检查式子两边的各种原子的个数及电荷数是否相等;
A.乙酸根离子水解是可逆反应;
B.氯气的氧化性大于过氧化氢;
C.将相互接触的铜片和锌片置于稀硫酸中,构成原电池,锌为原电池的负极;
D.硫化铜的溶解度小于氢氧化铜.
解答:解:A.在CH3COONa溶液中乙酸钠为强碱弱酸盐水解呈碱性,滴加酚酞变红,水解为可逆反应,离子方程式为CH3COO-+H2O?CH3COOH+OH-,故A错误;
B.氯气的氧化性大于过氧化氢,过氧化氢不能氧化氯离子生成氯气,FeCl3溶液能催化H2O2溶液,正确反应为:2H2O2
2H2O+O2↑,故B错误;
C.将相互接触的铜片和锌片置于稀硫酸中,构成铜锌原电池,Zn活泼,则Zn作负极,Cu作正极,发生电池反应为Zn+H2SO4═ZnSO4+H2↑,铜片表面有气泡产生,离子方程式为:Zn+2H+═Zn2++H2↑,故C错误;
D.氢氧化铜为蓝色沉淀,硫化铜为黑色沉淀,氢氧化铜的溶解度大于硫化铜,向Cu(OH)2悬浊液中滴加Na2S溶液,发生Cu(OH)2(s)+S2-?CuS(s)+2OH--,故D正确;
故选D.
B.氯气的氧化性大于过氧化氢,过氧化氢不能氧化氯离子生成氯气,FeCl3溶液能催化H2O2溶液,正确反应为:2H2O2
| ||
C.将相互接触的铜片和锌片置于稀硫酸中,构成铜锌原电池,Zn活泼,则Zn作负极,Cu作正极,发生电池反应为Zn+H2SO4═ZnSO4+H2↑,铜片表面有气泡产生,离子方程式为:Zn+2H+═Zn2++H2↑,故C错误;
D.氢氧化铜为蓝色沉淀,硫化铜为黑色沉淀,氢氧化铜的溶解度大于硫化铜,向Cu(OH)2悬浊液中滴加Na2S溶液,发生Cu(OH)2(s)+S2-?CuS(s)+2OH--,故D正确;
故选D.
点评:本题考查离子方程式的书写,明确发生的反应并熟悉离子反应方程式的书写方法是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
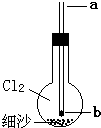 (2013?房山区一模)如图所示实验装置,烧瓶内充满氯气,底部有一层细沙(不参与反应),玻璃导管下口b处塞有一小块钠.从a口伸入一根细铁丝把钠块捅下去,再用滴管从a口滴下一滴水,恰好落在钠块上,立即剧烈反应.下列对此实验的说法中,不正确的是( )
(2013?房山区一模)如图所示实验装置,烧瓶内充满氯气,底部有一层细沙(不参与反应),玻璃导管下口b处塞有一小块钠.从a口伸入一根细铁丝把钠块捅下去,再用滴管从a口滴下一滴水,恰好落在钠块上,立即剧烈反应.下列对此实验的说法中,不正确的是( )