题目内容
【题目】下列离子方程式书写正确的是( )
A. 过量氨水滴入氯化铝溶液中:Al3++3OH―![]() Al(OH)3 ↓
Al(OH)3 ↓
B. 硫代硫酸钠溶液与稀硫酸混合:S2O32—+2H+![]() S↓+SO2↑+H2O
S↓+SO2↑+H2O
C. NaClO溶液与FeCl2溶液混合:2ClO―+Fe2++2H2O![]() 2HClO + Fe(OH)2 ↓
2HClO + Fe(OH)2 ↓
D. 次氯酸钙溶液中通入过量CO2 :Ca2+ +2ClO― +H2O +CO2 ![]() CaCO3↓+2HClO
CaCO3↓+2HClO
【答案】B
【解析】选项A中一水合氨是弱碱,在离子方程式中不能拆分为离子,所以选项A错误。硫代硫酸钠溶液与稀硫酸混合,生成硫酸钠、硫单质、二氧化硫和水,所以对应的离子方程式为:S2O32—+2H+![]() S↓+SO2↑+H2O,选项B正确。NaClO溶液有很强的氧化性,可以与FeCl2溶液发生氧化还原反应将Fe2+氧化,所以选项C错误。次氯酸钙溶液中通入过量CO2最后应该得到碳酸氢钙,选项D错误。
S↓+SO2↑+H2O,选项B正确。NaClO溶液有很强的氧化性,可以与FeCl2溶液发生氧化还原反应将Fe2+氧化,所以选项C错误。次氯酸钙溶液中通入过量CO2最后应该得到碳酸氢钙,选项D错误。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10﹣5molL﹣1 | K1=4.4×10﹣7molL﹣1 | 3.0×10﹣8 |
请回答下列问题:
(1)同浓度的CH3COO﹣、HCO3﹣、CO32﹣、ClO﹣结合H+的能力由强到弱的顺序为 .
(2)常温下0.1molL﹣1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是(填字母序号,下同).
A.c(H+) B. ![]() C.c(H+)c(OH﹣)
C.c(H+)c(OH﹣)
D. ![]() E.
E. ![]()
若该溶液升高温度,上述5种表达式的数据增大的是 .
(3)体积为10mL pH=2的醋酸溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程pH变化如图:
则HX的电离平衡常数(填“大于”、“等于”或“小于”)醋酸的平衡常数.稀释后,HX溶液中由水电离出来的c(H+)(填“大于”、“等于”或“小于”)醋酸的溶液中由水电离出来的c(H+),理由是 .
(4)已知100℃时,水的离子积为1×10﹣12 , 该温度下测得某溶液pH=7,该溶液显(填“酸”、“碱”或“中”)性.将此温度下pH=1的H2SO4溶液aL与pH=11的NaOH溶液bL混合,若所得混合液pH=2,则a:b= .
【题目】用如图所示装置进行下列实验,实验结果与预测的现象不一致的是
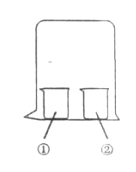
选项 | ① | ② | 现象 |
A | 淀粉KI溶液 | 浓硫酸 | 溶液变蓝 |
B | 酚酞溶液 | 浓盐酸 | 无明显变化 |
C | AlCl3溶液 | 浓氨水 | 有白色沉淀 |
D | 浓盐酸 | 浓氨水 | 有白烟产生 |
A. A B. B C. C D. D