题目内容
 生产硫酸最古老的方法是以绿矾为原料,在蒸馏釜中煅烧.反应的化学方程式为:
生产硫酸最古老的方法是以绿矾为原料,在蒸馏釜中煅烧.反应的化学方程式为:2FeSO4?7H2O
| ||
分析:A、二氧化硫和氯化钡不反应,不能生成亚硫酸钡沉淀;
B、石蕊试液只能检验氢离子的存在;
C、需要检验的是二氧化硫,c试管中需要加入品红试液检验;
D、依据三氧化硫和水的量,结合三氧化硫和水反应后形成的硫酸溶液计算质量分数;
B、石蕊试液只能检验氢离子的存在;
C、需要检验的是二氧化硫,c试管中需要加入品红试液检验;
D、依据三氧化硫和水的量,结合三氧化硫和水反应后形成的硫酸溶液计算质量分数;
解答:解:A、若将反应后的三种气体通入BaCl2溶液中,产生的沉淀为BaSO4,二氧化硫不能喝氯化钡反应,故A错误;
B、b中产物用紫色石蕊试液能检验出氢离子的存在,但检验不出硫酸根离子,故B错误;
C、氢氧化钠只能吸收二氧化硫无现象判断,应用品红试液检验,故C错误;
D、化学反应中生成1molSO3,14molH2O,发生SO3+H2O=H2SO4;反应后溶液中含13molH2O;1molH2SO4;溶质质量分数=
=29.5%;故D正确;
故选D.
B、b中产物用紫色石蕊试液能检验出氢离子的存在,但检验不出硫酸根离子,故B错误;
C、氢氧化钠只能吸收二氧化硫无现象判断,应用品红试液检验,故C错误;
D、化学反应中生成1molSO3,14molH2O,发生SO3+H2O=H2SO4;反应后溶液中含13molH2O;1molH2SO4;溶质质量分数=
| 1mol×98g/mol |
| 1mol×98g/mol+13mol×18g/mol |
故选D.
点评:本题考查了绿矾制硫酸的反应原理和产物的性质检验,溶液质量分数的计算,主要是二氧化硫、三氧化硫性质的应用.

练习册系列答案
相关题目


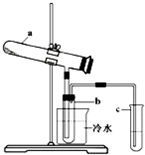
 Fe2O3+SO2+SO3↑+14H2O。其中三氧化硫与水蒸气同时冷凝便得到硫酸。用如图所示装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫(加热装置已略去)。其中b为干燥的试管。
Fe2O3+SO2+SO3↑+14H2O。其中三氧化硫与水蒸气同时冷凝便得到硫酸。用如图所示装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫(加热装置已略去)。其中b为干燥的试管。
