题目内容
【题目】将100 mL 2 mol/L AlCl3溶液跟一定体积4 mol/L NaOH溶液混合后可得7.8 g沉淀,则NaOH溶液的体积可能是:①75 mL ②150 mL ③175 mL ④200 mL
A. ① B. ② C. ①③ D. ②③
【答案】C
【解析】
![]()
![]()
![]() 溶液中
溶液中![]() ,若只发生反应:
,若只发生反应:![]() ↓
↓![]() ,生成氢氧化铝为
,生成氢氧化铝为![]() ,其质量
,其质量![]() ,说明有两种情况:一为沉淀不完全,只生成
,说明有两种情况:一为沉淀不完全,只生成![]() 沉淀;另一种情况为铝离子完全沉淀后部分溶解,既生成
沉淀;另一种情况为铝离子完全沉淀后部分溶解,既生成![]() 沉淀,又生成
沉淀,又生成![]() 。①若碱不足,只发生
。①若碱不足,只发生![]() ═
═![]() ↓,可以知道NaOH的物质的量为
↓,可以知道NaOH的物质的量为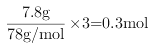 ,加入NaOH溶液的体积为
,加入NaOH溶液的体积为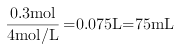 ;②沉淀部分溶解,既生成
;②沉淀部分溶解,既生成![]() 沉淀,又生成
沉淀,又生成![]() ,则;
,则;
![]() ═
═![]() ↓
↓
![]()
则溶解的氢氧化铝为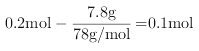 ,
,
![]() ═
═![]()
![]()
![]()
则消耗的碱的物质的量为![]() ,加入NaOH溶液的体积为
,加入NaOH溶液的体积为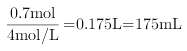 ;故选C。
;故选C。

练习册系列答案
相关题目
【题目】已知Ksp(CaCO3)=2.8×10-9及表中有关信息:
弱酸 | CH3COOH | H2CO3 |
电离平衡常数(常温) | Ka=1.8×10-5 | Ka1=4.3×10-7; Ka2=5.6×10-11 |
下列判断正确的是
A. 向Na2CO3溶液中滴入酚酞,溶液变红,主要原因是CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
B. 常温时,CH3COOH与CH3COONa混合溶液的pH=6,则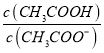 =18
=18
C. NaHCO3溶液中:c(OH-)-c(H+)=c(H2CO3)-c(CO32-)
D. 2×10-4 mol/L的Na2CO3溶液与CaCl2溶液等体积混合出现沉淀,则CaCl2溶液的浓度一定是5.6×10-5 mol/L

