题目内容
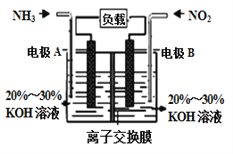
【题目】氮氧化物具有不同程度的毒性,会破坏人体的中枢神经,长期吸入会引起脑性麻痹,手脚萎缩等,大量吸入时会引发中枢神经麻痹,记忆丧失,四肢瘫痪,甚至死亡等后果。构成电池方法既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,发生反应6NO2+8NH3= 7N2+12H2O,装置如图所示。下列关于该电池的说法正确的是 ( )
A. 电子从右侧电极经过负载后流向左侧电极
B. 为使电池持续放电,离子交换膜需选用阴离子交换膜
C. 电极A极反应式为2NH3-6e-=N2+6H+
D. 当有4.48LNO2被处理时,转移电子物质的量为0.8mol
【答案】B
【解析】由反应6NO2+8NH3= 7N2+12H2O 可以知道,反应中NO2为氧化剂, NH3为还原剂,则A为负极,B为正极,负极发生氧化反应,正极发生还原反应,结合电解质溶液呈碱性解答该题。
由反应6NO2+8NH3= 7N2+12H2O 可以知道,反应中NO2为氧化剂, NH3为还原剂,则A为负极,B为正极;电子由负极经导线流向正极,A错误;原电池工作时,阴离子向负极移动,为使电池持续放电,离子交换膜需选用阴离子交换膜,防止二氧化氮反应生成硝酸盐和亚硝酸盐,导致原电池不能正常工作,B正确;电解质溶液呈碱性,则负极电极方程式为:2NH3-6e-+6OH-=N2+3H2O,C错误;没有给出气体所处的外界条件是否为标况下,无法利用气体摩尔体积进行计算,D错误;正确选项B。

练习册系列答案
相关题目