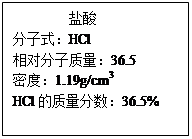题目内容
用于提纯或分离物质的方法有:
| A.萃取分液; | B.加热分解; | C.蒸发结晶; | D.分液;E、蒸馏;F、过滤等,请将提纯或分离方法的序号填在后面横线上。 |
(2)分离水和汽油的混合物___
(3)分离相溶的CCl4(沸点:76.75℃)和甲苯(沸点:110.6℃)的混合物_____
A D E
解析试题分析:(1)分离溶液中的溶质和溶剂,可利用溶质在互不相容的溶剂里的溶解度的不同,用一种溶剂把它从另一种溶剂里提取出来的方法叫萃取。从碘水里提取碘可用萃取的方法。选项为A。(2)分离互不相容的两种液体用分液的方法分离。分离水和汽油的混合物用分液法分离。选项为D。(3)分离互溶的、沸点相差较大的混合物可用蒸馏法分离。CCl4和甲苯互溶,沸点差别较大,用蒸馏法分离。选项为:E。
考点:考查常用的混合物的分离方法的知识。

 星级口算天天练系列答案
星级口算天天练系列答案为探究某抗酸药X的组成,进行如下实验:
查阅资料:
①抗酸药X可能的组成可以表示为:MgmAln(OH)p(CO3)q(SiO3)r(m、n、p、q、r为≥0的整数)。
② 在pH=5.0时沉淀完全;
在pH=5.0时沉淀完全; 在pH=8.8时开始沉淀,pH=11.4时沉淀完全。
在pH=8.8时开始沉淀,pH=11.4时沉淀完全。
实验过程:
| 步骤 | 实验操作 | 实验现象 |
| I | 向X的粉末中加入过量盐酸 | 产生气体A,得到无色溶液 |
| II | 向Ⅰ所得的溶液中滴加氨水,调节pH至5~ 6,过滤 | 生成白色沉淀B |
| III | 向沉淀B中加过量NaOH溶液 | 沉淀全部溶解 |
| IV | 向II得到的滤液中滴加NaOH溶液,调节pH至12 | 生成白色沉淀C |
(1)Ⅰ中气体A可使澄清石灰水变浑浊,A的化学式是 。
(2)II中生成B反应的离子方程式是 。
(3)III中B溶解反应的离子方程式是 。
(4)沉淀C的化学式是 。
(5)若上述n(A)︰n(B)︰n(C)=1︰2︰3,则X的化学式是 。
现有失去标签的CaCl2、AgNO3、HCl、和Na2CO3四瓶溶液。为了确定四种溶液的成分,将它们编号为A、B、C、D后进行化学实验。实验记录如下:
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A + B | 无明显现象 |
| ② | B + D | 有无色无味气体放出 |
| ③ | C + B | 有白色沉淀生成 |
| ④ | A + D | 有白色沉淀生成 |
根据上述实验完成下列各小题:
(1)A、B、C、D四瓶溶液分别是(用化学式表示所含溶质)
A B C D
(2)写出B与D反应的离子方程式
写出B与C反应的离子方程式
苯甲酸广泛应用于制药和化工行业,某兴趣小组同学利用高锰酸钾氧化甲苯制备苯甲酸(KMnO4中性条件下还原产物为MnO2,酸性条件下为Mn2+)
已知:苯甲酸相对分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3 g和6.9 g。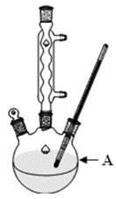
实验流程:
①往装置A中加入2.7mL(2.3 g)甲苯和125 mL水,然后分批次加入8.5 g稍过量的KMnO4固体,控制反应温度约在100℃,当甲苯层近乎消失,回流不再出现油珠时,停止加热。
②将反应混合物趁热过滤,用少量热水洗涤滤渣,合并滤液与洗涤液,冷却后加入浓盐酸,经操作I得白色较干燥粗产品。
③纯度测定:称取1.220g白色样品,配成100mL,甲醇溶液,取25.00mL溶液,用0.1000mol/L KOH标准溶液滴定,重复滴定四次,每次消耗的体积如下表所示列举:
| | 第一次 | 第二次 | 第三次 | 第四次 |
| 体积(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
(1)装置A的名称 。若不用温度计,本实验控制反应温度的措施为 。
(2)白色粗产品中除了KCl外,其他可能的无机杂质为 。
(3)操作I的名称 。
(4)步骤③中用到的定量仪器有 ,100mL容量瓶,50mL酸式、碱式滴定管。
(5)样品中苯甲酸纯度为 。
(6)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则测定结果 (填“偏大”、“偏小”或“不变”)。