��Ŀ����
����Ŀ��ij����С��Ϊ�˼���Ũ������ľ̿�ڼ��������·�Ӧ������SO2��CO2���壬�������ͼ��ʾʵ��װ�ã�a��b��cΪֹˮ�У�B�����ڴ��������ң�D�з�����I2�͵��۵���ɫ��Һ��ʪ����֬�ޣ� 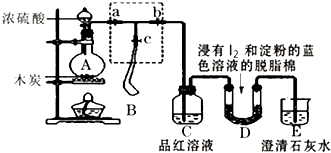
��1��װ��A��ʢ��Ũ������������� ��
��2��װ��A�з�����Ӧ�Ļ�ѧ����ʽΪ ��
��3��ʵ��ʱ��װ��C�е�����Ϊ ��
��4����ʵ��ɰܵĹؼ����ڿ��Ʒ�Ӧ������������ʲ��ܹ��죬����������ֵ�װ�ã�����ȷ�IJ���˳�������ò��������д���� ����Aװ���м���Ũ���ᣬ���ȣ�ʹA�в����������������B���������г���һ��������ʱ��ֹͣ���ȣ�
�ڴ�װ��A��ȴ��������B��������ٱ仯�ر�ֹˮ��a����ֹˮ��b��������ѹ���ң�ʹ����B��������������װ��C�У����ﵽʵ��Ŀ�ĺر�ֹˮ��b��
�۴�ֹˮ��a��c���ر�ֹˮ��b��
��5����D�в�������ʱ������˵��ʹE�г���ʯ��ˮ����ǵ���CO2 �� ������SO2��д��D�з�����Ӧ�Ļ�ѧ����ʽ �� ��D�з�Ӧ����0.3mol����ת��ʱ��������Ӧ��������������״������L��
���𰸡�
��1����Һ©��
��2��C+2H2SO4��Ũ�� ![]() CO2��+2SO2��+2H2O
CO2��+2SO2��+2H2O
��3��Ʒ����Һ��ɫ
��4���ۢ٢�
��5��������һ����֬����ɫ��dz��������һ����֬����ɫ���䣻I2+SO2+2H2O=H2SO4+2HI��3.36
���������⣺��1��װ��A��ʢ��Ũ�������������Ϊ��Һ©�������Դ��ǣ���Һ©������2��װ��A��Ũ������ǿ�����ԣ��ܽ�C����Ϊ������̼����Ӧ�Ļ�ѧ����ʽΪC+2H2SO4��Ũ�� ![]() CO2��+2SO2��+2H2O�����Դ��ǣ�C+2H2SO4��Ũ��
CO2��+2SO2��+2H2O�����Դ��ǣ�C+2H2SO4��Ũ�� ![]() CO2��+2SO2��+2H2O����3�������������Ư���ԣ�����C��Ʒ����Һ��ɫ�����Դ��ǣ�Ʒ����Һ��ɫ����4������B���������ռ����壬Ҫ��������٣������߿����������Ӧ���ռ����壬Ȼ���������ͷ����壬������ȷ�IJ���˳��Ϊ���ۢ٢ڣ����Դ��ǣ��ۢ٢ڣ���5����Dװ���н�����һ����֬����ɫ��dz��������һ����֬����ɫ����ʱ�������ڳ����Ƕ�����̼���ⵥ���ܽ�������������Ϊ���ᣬ��Ӧ�Ļ�ѧ����ʽΪ��I2+SO2+2H2O=H2SO4+2HI����Ӧ�е���ת��2e��������Ӧ����������������ʵ���Ϊ1mol����D�з�Ӧ����0.3mol����ת��ʱ��������Ӧ����������ʵ���=0.15mol���������״����=22.4L/mol��0.15mol=3.36L�����Դ��ǣ�������һ����֬����ɫ��dz��������һ����֬����ɫ���䣻I2+SO2+2H2O=H2SO4+2HI�� 3.36��
CO2��+2SO2��+2H2O����3�������������Ư���ԣ�����C��Ʒ����Һ��ɫ�����Դ��ǣ�Ʒ����Һ��ɫ����4������B���������ռ����壬Ҫ��������٣������߿����������Ӧ���ռ����壬Ȼ���������ͷ����壬������ȷ�IJ���˳��Ϊ���ۢ٢ڣ����Դ��ǣ��ۢ٢ڣ���5����Dװ���н�����һ����֬����ɫ��dz��������һ����֬����ɫ����ʱ�������ڳ����Ƕ�����̼���ⵥ���ܽ�������������Ϊ���ᣬ��Ӧ�Ļ�ѧ����ʽΪ��I2+SO2+2H2O=H2SO4+2HI����Ӧ�е���ת��2e��������Ӧ����������������ʵ���Ϊ1mol����D�з�Ӧ����0.3mol����ת��ʱ��������Ӧ����������ʵ���=0.15mol���������״����=22.4L/mol��0.15mol=3.36L�����Դ��ǣ�������һ����֬����ɫ��dz��������һ����֬����ɫ���䣻I2+SO2+2H2O=H2SO4+2HI�� 3.36��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ������Ϊ�����л�����й���Ϣ�����ݱ�����Ϣ�ش����⣮
A | B | C |
�������������һ�����ҵ�ʯ�ͻ���ˮƽ | ����ģ��Ϊ�� | ������Ҫ�ɷ� |
��1��A�ṹ��ʽ�� �� ��������ʹ���Ը��������Һ��������Ȼ�̼��Һ��ɫ�����У����������ܷ����ķ�Ӧ�����Ӧ���ͣ������巴Ӧ�Ļ�ѧ����ʽΪ �� ��������Ȼ�̼��Һ��������2.8gʱ�������������Ϊ ��
��2����ҵ�ϣ�B��Դ��ú������Һ̬����ú���ͣ�B��Ũ���ᷢ��ȡ����Ӧ���÷�Ӧ�Ļ�ѧ����ʽΪ ��
��3��C��������Ӧ�����ɶ��ȴ����д���÷�Ӧ�Ļ�ѧ����ʽΪ ��
����Ŀ����ͼ������������̽��SO2�����ʣ�ʵ��ʱ��Na2SO3�����ϵμ���Ũ���ᣬ��������һ����������档���ж�ʵ���������������Ͳ���ȷ����

ѡ�� | ʵ������ | ���� |
A | BaCl2��Һ����� | SO2��BaCl2��Һ��Ӧ������BaSO3���� |
B | Na2S��Һ����� | SO2��Na2S��Һ��Ӧ������S���� |
C | ����KMnO4��Һ��ɫ | SO2���л�ԭ�� |
D | Ʒ����Һ��ɫ | SO2����Ư���� |
A. A B. B C. C D. D