题目内容
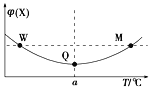
【题目】在某2 L恒容密闭容器中充入2 mol X(g)和1 mol Y(g)发生反应:2X(g)+Y(g)![]() 3Z(g) ΔH,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
3Z(g) ΔH,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
A. M点时,Y的转化率最大
B. W、M两点Y的正反应速率相等
C. 升高温度,平衡常数减小
D. 平衡后充入Z达到新平衡时Z的体积分数增大
【答案】C
【解析】温度在a℃之前,升高温度,X的含量减小,温度在a℃之后,升高温度,X的含量增大,曲线上最低点为平衡点,最低点之前未达平衡,反应向正反应进行,最低点之后,各点为平衡点,升高温度X的含量增大,平衡向逆反应方向移动,故正反应为放热反应。A.曲线上最低点Q为平衡点,升高温度平衡向逆反应移动,Y的转化率减小,所以Q点时,Y的转化率最大,故A错误;B.W点对应的温度低于M点对应的温度,温度越高,反应速率越高,所以W点Y的正反应速率小于M点Y的正反应速率,故B错误;C.根据上述分析,该反应为放热反应,升高温度,平衡逆移,平衡常数减小,故C正确;D.反应前后气体的物质的量不变,平衡时充入Z,达到平衡时与原平衡是等效平衡,所以达到新平衡时Z的体积分数不变,故D错误;故选C。

练习册系列答案
相关题目
【题目】化学与生活,生产息息相关。下列有关物质用途及原理分析都正确且有相关性的是( )
选项 | 物质用途 | 原理分析 |
A | 液氨常作制冷剂 | 氨气分解生成N2和H2是吸热反应 |
B | 聚碳酸酯料替代聚乙烯作包装材料 | 聚碳酸酯塑料容易降解成小分子 |
C | 磁性氧化铁用于制造指南针 | Fe2O3具有磁性 |
D | 服用豆浆可缓解重金属中毒 | 重金属使蛋白质盐析 |
A. AB. BC. CD. D
