题目内容
3.下列性质的比较中,正确的是( )| A. | 氧化性:S>Cl2 | B. | 金属性:K<Na | ||
| C. | 热稳定性:NaHCO3>Na2CO3 | D. | 酸性:HClO4>H2SO4 |
分析 A、元素的非金属性越强,对应单质的氧化性越强;
B、同主族从上往下金属性增强;
C、NaHCO3不稳定,加热易分解;
D、非金属性越强,最高价氧化物对应水化物的酸性越强.
解答 解:A、元素的非金属性:Cl>S,所以单质的氧化性:S<Cl2,故A错误;
B、同主族从上往下金属性增强,所以金属性:K>Na,故B错误;
C、NaHCO3不稳定,加热易分解:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,碳酸钠受热稳定,故C错误;
D.非金属性:Cl>S,所以酸性:HClO4>H2SO4,故D正确;
故选D.
点评 本题考查元素周期律知识,侧重于学生的分析能力和基本概念的理解和运用的考查,注意元素的性质与对应单质、化合物的关系,把握元素周期律的递变规律是解答该类题目的关键,难度不大.

练习册系列答案
相关题目
14.N2O是一种氧化剂,有轻微麻醉作用.并能致人发笑,可采取以下方法制备:3CO+2NO2═3CO2+N2O.下列说法正确的是( )
| A. | 每生成lmolN2O,转移3mol电子 | |
| B. | 等质量的N2O和CO2两种分子,物质的量、原子总数、电子数和质子数相同 | |
| C. | 只有氧化性,没有还原性 | |
| D. | 每生成1molN2O,消耗67.2L CO |
11.从化学的角度将下列物质进行分类,下列说法正确的是( )
| A. | CO与CO2互为同素异形体 | B. | 金刚石与石墨互为同分异构体 | ||
| C. | 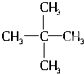 与 与 是同分异构体 | D. | 冰与水互为同分异构体 |
18.下列物质既属于钠盐又属于硫酸盐的是( )
| A. | 碳酸钾 | B. | 硫酸钾 | C. | 碳酸钠 | D. | 硫酸钠 |
8.下列有关胶体的叙述正确的是( )
| A. | 胶体粒子的大小通常在0.1~1nm之间 | |
| B. | 阳光穿透清晨的树林时形成的光柱,是胶体的丁达尔效应的体现 | |
| C. | 可以通过过滤分离溶液和胶体 | |
| D. | 向FeCl3溶液中加入NaOH溶液,会出现红褐色Fe(OH)3胶体 |
15.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 18g水中含有的原子数为2NA | |
| B. | 11.2L O2一定含有NA个原子 | |
| C. | 标准状况下,NA个水分子所占体积为22.4L | |
| D. | NA个氧分子和NA个氢分子的质量比等于16:1 |
13.某烃的结构简式如图所示,它的正确命名应是( )
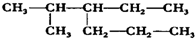
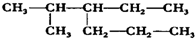
| A. | 2-甲基-3-丙基戊烷 | B. | 3-异丙基己烷 | ||
| C. | 2-甲基-3-乙基己烷 | D. | 5-甲基-4-乙基戊烷 |