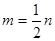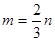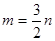题目内容
实验室用Zn与稀H2SO4反应来制取氢气,常加少量CuSO4来加快反应速率。为了研究CuSO4的量对H2生成速率的影响,某同学用实验比较法设计了如下实验方案,将表中所给的试剂按一定体积混合后,分别加入四个盛有相同大小的Zn片(过量)的反应瓶(甲、乙、丙、丁)中,收集产生的气体,并记录收集相同体积的气体所需的时间。
下列说法正确的是
A.t1 < t2 < t3 < t4 B.V4=V5=10 C.V6=7.5 D.V1<V2<V3<20
| 实验 试剂 | 甲 | 乙 | 丙 | 丁 |
| 4 mol·L-1H2SO4/mL | 20 | V1 | V2 | V3 |
| 饱和CuSO4溶液/mL | 0 | 2.5 | V4 | 10 |
| H2O/mL | V5 | V6 | 8 | 0 |
| 收集气体所需时间/s | t1 | t2 | t3 | t4 |
A.t1 < t2 < t3 < t4 B.V4=V5=10 C.V6=7.5 D.V1<V2<V3<20
C
因为该实验是来研究硫酸铜的量对氢气生成速率的影响,因此要保证锌和硫酸完全一致,即V1、V2、V3均是20ml。要保证实验中硫酸的浓度相等,由实验丁可知所加饱和硫酸铜溶液的体积和水的体积之和一定是10ml,所以V6=7.5ml,V5=10ml,V4=2ml。因为实验甲中不能构成原电池,反应慢,用时多,所以正确的答案是C。

练习册系列答案
相关题目
 2SO3(g) ΔH<0在一定条件下达到平衡状态,时间为t1时改变条件。化学反应速率与反应时间关系如图。下列说法中正确的是
2SO3(g) ΔH<0在一定条件下达到平衡状态,时间为t1时改变条件。化学反应速率与反应时间关系如图。下列说法中正确的是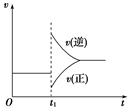
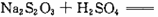
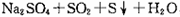 ,下列各组实验中最先出现浑浊是( )
,下列各组实验中最先出现浑浊是( )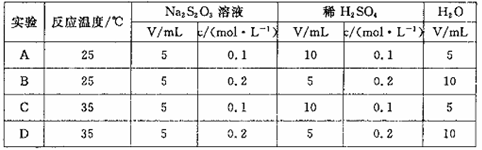
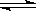 2NH3在10L密闭容器中进行,测得2min内,N2的物质的量由20mol减少到8mol,则2min内N2的平均反应速率为
2NH3在10L密闭容器中进行,测得2min内,N2的物质的量由20mol减少到8mol,则2min内N2的平均反应速率为 2HCN(g) + 6H2O(g)反应中,已知v (HCN) =" n" mol/(L·min),且v(O2) =" m" mol/(L·min),则m与n的关系正确的是
2HCN(g) + 6H2O(g)反应中,已知v (HCN) =" n" mol/(L·min),且v(O2) =" m" mol/(L·min),则m与n的关系正确的是