题目内容
(1)已知:25℃时,一些弱电解质的电离常数如下:NH3·H2O:1.77×10—5 H2CO3:4.3×10—7(第一步电离)。则:NH4HCO3溶液显 性 。
(2)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈 性,醋酸体积 (填“>”、“<”、“=”)氢氧化钠溶液体积。
(3)电解质A的化学式为NanB,测得浓度为c mol/L的A溶液的pH=10,A溶液呈碱性的原因是(用离子方式程式表示)________________
(4)污水中含有Hg2+,用难溶的FeS作为沉淀剂可使Hg2+转化为HgS而除去,该反应能进行的依据是: ;有人认为加入FeS作为沉淀剂还可以起到净化水的作用,请您运用所学知识解释
(5)已知Ksp(AB2)=4.2×10-8,Ksp(AC)=3.0×10—15。在AB2、AC均为饱和的混合液中,测得c(B—)=1.6×10—3 mol·L-1,则溶液中c(C2—)为 mol/L。
(2)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈 性,醋酸体积 (填“>”、“<”、“=”)氢氧化钠溶液体积。
(3)电解质A的化学式为NanB,测得浓度为c mol/L的A溶液的pH=10,A溶液呈碱性的原因是(用离子方式程式表示)________________
(4)污水中含有Hg2+,用难溶的FeS作为沉淀剂可使Hg2+转化为HgS而除去,该反应能进行的依据是: ;有人认为加入FeS作为沉淀剂还可以起到净化水的作用,请您运用所学知识解释
(5)已知Ksp(AB2)=4.2×10-8,Ksp(AC)=3.0×10—15。在AB2、AC均为饱和的混合液中,测得c(B—)=1.6×10—3 mol·L-1,则溶液中c(C2—)为 mol/L。
(1)(1分)碱
(2)(1分)中性,(1分)>
(3)(2分)Bn-+H2O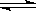 HB(n-1)-+OH-
HB(n-1)-+OH-
(4)Ksp(HgS)<Ksp(FeS);因发生Hg2++FeS=HgS+Fe2+,产生的Fe2+可被氧化为Fe3+,Fe3+水解形成Fe(OH)3胶体,吸附杂质而净化水(每空2分,共4分)
(5)(2分)1.83×10—13
(2)(1分)中性,(1分)>
(3)(2分)Bn-+H2O
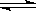 HB(n-1)-+OH-
HB(n-1)-+OH-(4)Ksp(HgS)<Ksp(FeS);因发生Hg2++FeS=HgS+Fe2+,产生的Fe2+可被氧化为Fe3+,Fe3+水解形成Fe(OH)3胶体,吸附杂质而净化水(每空2分,共4分)
(5)(2分)1.83×10—13
试题分析:(1)NH3·H2O:1.77×10—5 H2CO3:4.3×10—7(第一步电离),这说明了碳酸氢根离子的水解程度比铵根离子更加弱,所以其水解程度较大,故NH4HCO3溶液显碱性;2)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,根据电荷守恒可以得到:c(CH3COO-)+ c(OH-)=c(Na+)+ c(H+),因为c(CH3COO-)=c(Na+),所以 c(OH-)=c(H+),故混合后溶液呈中性,醋酸体积>氢氧化钠溶液体积;(3)电解质A的化学式为NanB,测得浓度为c mol/L的A溶液的pH=10,说明了B离子发生了水解,其离子方程式为Bn-+H2O
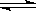 HB(n-1)-+OH-;(4)污水中含有Hg2+,用难溶的FeS作为沉淀剂可使Hg2+转化为HgS而除去,该反应能进行的依据是:Ksp(HgS)<Ksp(FeS);FeS作为沉淀剂还可以起到净化水的作用,其原因为因发生Hg2++FeS=HgS+Fe2+,产生的Fe2+可被氧化为Fe3+,Fe3+水解形成Fe(OH)3胶体,吸附杂质而净化水;(5)因为Ksp(AB2)=4.2×10-8,Ksp(AC)=3.0×10—15,c(B—)=1.6×10—3 mol·L-1,AB2、AC均为饱和的混合液,即c2(B—)c(A—)=4.2×10-8,所以c(A2+)=1.64×10—2mol·L-1,
HB(n-1)-+OH-;(4)污水中含有Hg2+,用难溶的FeS作为沉淀剂可使Hg2+转化为HgS而除去,该反应能进行的依据是:Ksp(HgS)<Ksp(FeS);FeS作为沉淀剂还可以起到净化水的作用,其原因为因发生Hg2++FeS=HgS+Fe2+,产生的Fe2+可被氧化为Fe3+,Fe3+水解形成Fe(OH)3胶体,吸附杂质而净化水;(5)因为Ksp(AB2)=4.2×10-8,Ksp(AC)=3.0×10—15,c(B—)=1.6×10—3 mol·L-1,AB2、AC均为饱和的混合液,即c2(B—)c(A—)=4.2×10-8,所以c(A2+)=1.64×10—2mol·L-1,c(C2—)=Ksp(AC)/c(A2+)=3.0×10—15/1.64×10—2=1.83×10—13mol·L-1。
点评:本题考查了盐类水解,电荷守恒、溶度积的计算,这些知识是高考考查的重点和难点,本题有一定的综合性,难度适中。

练习册系列答案
相关题目
 增大
增大 )>c(A-)>c(B-)>c(H+) B.c(OH—)>c(HA)>c(HB)>c(H+)
)>c(A-)>c(B-)>c(H+) B.c(OH—)>c(HA)>c(HB)>c(H+)