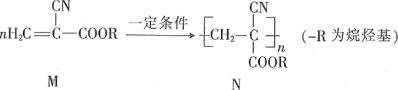
题目内容
【题目】如图是元素周期表的一部分,表中所列字母分别代表一种元素。根据表中所列元素回答下列问题:
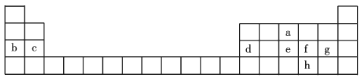
(1)元素d在元素周期表中的位置是________,元素h与f的原子序数相差_____。
(2)元素b、c、f形成的简单离子中半径最小的是______(填离子符号),原子半径最小的是______(填元素符号)。
(3)表中第三周期所列元素的非金属性最强的是______(填元素符号),e、f、g三种元素的简单氢化物中最不稳定的是______(填化学式)。
(4)元素![]() 与元素
与元素![]() 的最高价氧化物对应水化物反应的化学方程式为______。
的最高价氧化物对应水化物反应的化学方程式为______。
(5)铅(Pb)、锡(Sn)、锗(Ge)与碳(C)、硅(Si)属于同主族元素,常温下,在空气中,单质锡、锗均不反应而单质铅表面生成一层氧化铅;单质锗与盐酸不反应,而单质锡与盐酸反应。由此可得出以下结论:
①锗的原子序数为______;
②铅(Pb)、锡(Sn)、锗(Ge)的+4价氢氧化物的碱性由强到弱的顺序为___________(用化学式表示)。
(6)最近,德国科学家实现了铷原子气体的超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷(Rb)是37号元素,相对原子质量是85.5,与钠同主族。回答下列问题:
①铷在元素周期表中的位置为__________________。
②同主族元素的同类化合物的性质相似,请写出AlCl3与RbOH过量反应的离子方程式:_____________________。
③现有铷和另一种碱金属形成的混合金属50 g,当它与足量水反应时,放出标准状况下的氢气22.4 L,另一种碱金属可能是__________。(填序号)
A.Li B.Na C.K D.Cs
【答案】第三周期第ⅢA族 18 Mg2+ S Cl PH3 NaOH+HClO4=NaClO4+H2O 32 Pb(OH)4>Sn(OH)4>Ge(OH)4 第五周期第ⅠA族 Al3++4OH-=AlO2-+2H2O (或写为Al3++4OH-=[Al(OH)4]-) AB
【解析】
由元素在周期表的位置可知,a是N元素,b为Na元素,C为Mg元素,d为Al元素,e为P元素,f为S元素,g为Cl元素,h为Se元素,然后根据元素周期律分析解答。
根据元素在周期表的位置可知确定各种元素分别是:a是N元素,b为Na元素,C为Mg元素,d为Al元素,e为P元素,f为S元素,g为Cl元素,h为Se元素。
(1)元素d为Al,原子核外电子排布是2、8、3,所以在元素周期表中的位置是第三周期IIIA族,f是16号元素S,h是34号元素Se,h与f原子序数相差34-16=18;
(2)b、c、f形成的简单离子分别是Na+、Mg2+、S2-,Na+、Mg2+核外电子排布为2、8,具有两个电子层,S2-核外电子排布是2、8、8,具有三个电子层,离子核外电子层数越多,离子半径越大,对于电子层结构相同的离子来说,核电荷数越大,离子半径越小,所以,三种离子中离子半径最小的是Mg2+;Na、Mg、S都是同一周期的元素,原子序数越大,原子半径越小,所以三种元素的原子半径最小的是S;
(3)同一周期的元素,原子序数越大,元素的非金属性越强,表中第三周期元素的非金属性最强是Cl;元素的非金属性越强,其简单氢化物的稳定性就越强,e、f、g三种元素分别表示P、S、Cl,元素的非金属性:P<S<Cl,所以它们形成的简单气态氢化物最不稳定的是PH3;
(4)g元素与b元素的最高价氧化物对应水化物分别是HClO4、NaOH,HClO4是一元强酸,NaOH是一元强碱,二者混合发生中和反应产生盐和水,反应的化学方程式为NaOH+HClO4=NaClO4+H2O;
(5)①锗位于Si元素下一周期,二者原子序数相差18,所以Ge的原子序数为14+18=32;
②由于同一主族的元素从上到下元素的金属性逐渐增强,所以根据铅(Pb)、锡(Sn)、锗(Ge)在元素周期表的位置可知,元素的金属性Pb>Sn>Ge,元素的金属性越强,其最高价氧化物对应水化物的碱性逐渐增强,故铅(Pb)、锡(Sn)、锗(Ge)的+4价氢氧化物的碱性由强到弱的顺序为Pb(OH)4>Sn(OH)4>Ge(OH)4;
(6)①铷(Rb)是37号元素,原子核外有5个电子层,最外层有1个电子,所以37号元素在元素周期表中的位置为第五周期第ⅠA族;
②铷(Rb)与钠同主族,由于Rb的金属性比Na强,所以RbOH是一元强碱,AlCl3与过量的RbOH反应产生的离子方程式为Al3++4OH-= AlO2-+2H2O (或写为Al3++4OH-=[Al(OH)4]-);
③22.4 L标准状况下的H2的物质的量n(H2)=22.4 L÷22.4 L/mol=1 mol,铷和水反应的化学方程式为2Rb+2H2O=2RbOH+H2↑,可知2 molRb反应产生1 mol H2,由碱金属与水反应的化学方程式为2M+2H2O=2MOH+H2↑可知混合金属的平均摩尔质量M=![]() =25 g/mol,Rb的摩尔质量为85.5 g/mol,则另一种碱金属的摩尔质量一定小于25 g/mol,所以另一种碱金属可能是Li或Na,故合理选项是AB。
=25 g/mol,Rb的摩尔质量为85.5 g/mol,则另一种碱金属的摩尔质量一定小于25 g/mol,所以另一种碱金属可能是Li或Na,故合理选项是AB。

【题目】已知X、Y、Z、W为原子序数依次增大的四种短周期主族元素,前三种元素原子的电子层数相同,Y、W元素原子的最外层电子数相同。表给出了四种元素的部分信息,则下列说法正确的是
元素 | X | Y | Z | W |
原子半径/nm | 0.134 | r1 | r2 | 0.106 |
A.r1>r2>0.106
B.0.134<r1<r2
C.0.134>r1>r2
D.电子层数多的元素的原子半径一定比较大
【题目】某化学课外活动小组为了验证元素化学性质递变规律,进行如下实验探究。
Ⅰ.探究1:验证同周期X、Y、Z三种元素金属性递变规律
实验内容 | 实验现象 |
1、各取1.0g金属X和金属Z,分别加入到5mL水中 | 金属X与水反应比金属Z剧烈 |
2、各取1.0g的金属Z和金属Y(形状相同),分别加入到5mL1.0mol/L盐酸中。 | 金属Z与盐酸反应比金属Y剧烈 |
通过实验验证三种元素金属性由强到弱是_____,则下列判断正确的是(__________)
A.原子序数:Y>Z>X B.原子的最外层电子数X>Y>Z
C.原子半径:Y>Z>X D.Y的最高价氧化物对应水化物的碱性最强
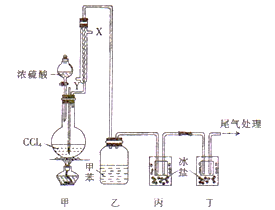
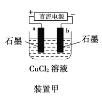
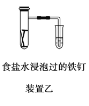
Ⅱ.探究2:验证氯元素的非金属性比硫元素的非金属性强,设计如下实验:

(1)装置A中盛放的试剂是_______(填选项),化学反应方程式是_________。
A.Na2SO3溶液 B.Na2S溶液 C.Na2SO4溶液
(2)下列不能用于验证氯元素比硫元素非金属性强的依据为______(填选项)。
A.HCl比H2S稳定
B.HClO氧化性比H2SO4强
C.HClO4酸性比H2SO4强
D.铁与Cl2反应生成FeCl3,而硫与铁反应生成FeS
(3)若要验证非金属性:Cl>I,装置A中加入淀粉碘化钾混合溶液,观察到装置A中溶液_______的现象,即可证明。用原子结构理论解释非金属性Cl>I的原因:同主族元素从上到下,________________。