题目内容
【题目】如图所示装置,若将胶头滴管中的水挤入集气瓶中,请描述观察到的现象并写出有关的离子方程式. 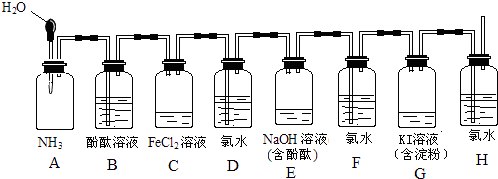
(1)A中的现象为 , 化学方程式 .
(2)C中的现象为 , 离子方程式 .
(3)E中的现象为 , 离子方程式 .
(4)G中的现象为 , 离子方程式 .
【答案】
(1)B中无色溶液倒吸入A中,且变为红色; NH3+H2O?NH3?H2O?
(2)溶液由浅绿色变为黄色;2Fe2++Cl2=2Fe3++2Cl﹣
(3)溶液红色褪去; Cl2+2OH﹣=Cl﹣+ClO﹣+H2O
(4)溶液变为蓝色; Cl2+2I﹣=I2+2Cl﹣
【解析】解:(1)氨气极易溶于水,将胶头滴管中的水挤入集气瓶,引发喷泉,则观察到B中无色溶液倒吸入A中,且变为红色,溶液变红是因发生电离反应为NH3H2ONH4++OH﹣,氨气与水反应生成一水合氨,方程式:NH3+H2ONH3H2O;所以答案是:B中无色溶液倒吸入A中,且变为红色;NH3+H2ONH3H2O;(2)氯水进入C中,发生氧化还原反应生成氯化铁,观察到C中溶液由浅绿色变为黄色,发生的离子反应为2Fe2++Cl2=2Fe3++2Cl﹣,
所以答案是:溶液由浅绿色变为黄色;2Fe2++Cl2=2Fe3++2Cl﹣;(3)氯水进入E中,发生氧化还原反应生成NaCl、NaClO和水,观察到E中溶液红色褪去,离子反应为Cl2+2OH﹣=Cl﹣+ClO﹣+H2O,所以答案是:溶液红色褪去;Cl2+2OH﹣=Cl﹣+ClO﹣+H2O;(4)氯水进入G中,与KI发生氧化还原反应生成碘单质,淀粉遇碘变蓝,观察到G中溶液变为蓝色,发生的离子反应为Cl2+2I﹣=I2+2Cl﹣,
所以答案是:溶液变为蓝色;Cl2+2I﹣=I2+2Cl﹣.
【考点精析】解答此题的关键在于理解氯气的化学性质的相关知识,掌握氯气的化学性质:与金属反应将金属氧化成高价态;非金属反应;与水反应;与碱反应;与还原性物质反应,以及对氨的化学性质的理解,了解与水反应,NH3是惟一能使润湿的红色石蕊试纸交蓝的气体,常用此性质检验NH3;与酸反应:NH3+HCl=NH4Cl(生成白烟);与O2反应:4NH3+5O2=4NO+6H2O+Q;

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】只给出表中甲和乙对应的量,不能用来求物质的量的是
甲 | 乙 | |
① | 物质微粒数 | 阿伏加德罗常数 |
② | 标准状况下气体摩尔体积 | 标准状况下气体体积 |
③ | 固体体积 | 固体密度 |
④ | 溶液质量分数 | 溶液体积 |
⑤ | 非标准状况下物质的质量 | 物质的摩尔质量 |
A. ②③④ B. ③④⑤ C. ③④ D. ④