题目内容
8.合成氨厂用氨气和空气的混合气体通过灼热铂-铑合金网发生氨氧化反应,若有标准状况下A L氨气完全反应.并转移电子数X个,则阿伏加德罗常数(NA)可表示为( )| A. | $\frac{11.2X}{5A}$mol-1 | B. | $\frac{5A}{11.2X}$mol-1 | C. | $\frac{22.4A}{5X}$mol-1 | D. | $\frac{22.4X}{5A}$mol-1 |
分析 发生反应:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,反应中N元素化合价由-3价升高为+2价,根据n=$\frac{V}{{V}_{m}}$计算氨气物质的量,结合N元素化合价变化表示出电子数目,进而计算阿伏伽德罗常数.
解答 解:发生反应:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,反应中N元素化合价由-3价升高为+2价,有标准状况下A L氨气完全反应,则转移电子数目为:$\frac{AL}{22.4L/mol}$×[2-(-3)]×NA=X,解得NA=$\frac{22.4X}{5A}$mol-1,故选D.
点评 本题考查阿伏伽德罗常数计算、氧化还原反应计算,关键是理解氧化还原反应中转移电子的计算,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.关于有机物的叙述正确的是( )
| A. | 丙烷的二卤代物是4种,则其六卤代物是2种 | |
| B. | 对二甲苯的核磁共振氢谱显示有3种化学环境的氢 | |
| C. | 甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有3种 | |
| D. | 某烃的同分异构体只能形成一种一氯代物,其分子式可能为C5H12 |
19.下列物质属于合成高分子化合物的是( )
| A. | 淀粉 | B. | 蚕丝 | C. | 聚氯乙烯 | D. | 纤维素 |
16.下列溶液中,有关物质的量浓度关系正确的是( )
| A. | 向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+ )=c(NO3 - ) | |
| B. | 1.0 mol•L-1Na2CO3 溶液:c(OH-)=c(HCO3-)+c(H+) | |
| C. | pH=8.0的KHS溶液中,c(K+)>c(HS-)>c(OH-)>c(S2-)>c(H+) | |
| D. | 将0.2 mol•L-1的某一元酸HA溶液和0.1 mol•L-1NaOH溶液等体积混合后,溶液pH大于7,则反应后的混合液中:2c(OH-)+c (A-)=2c(H+)+c(HA) |
3. 在密闭容器中,1molH2与1molCO发生反应:CO(g)+2H2(g)?CH3OH(g),△H<0,反应达到平衡时,改变温度(T)和压强(P),反应混合物中甲醇的物质的量分数变化情况如图所示,下列说法正确的是( )
在密闭容器中,1molH2与1molCO发生反应:CO(g)+2H2(g)?CH3OH(g),△H<0,反应达到平衡时,改变温度(T)和压强(P),反应混合物中甲醇的物质的量分数变化情况如图所示,下列说法正确的是( )
 在密闭容器中,1molH2与1molCO发生反应:CO(g)+2H2(g)?CH3OH(g),△H<0,反应达到平衡时,改变温度(T)和压强(P),反应混合物中甲醇的物质的量分数变化情况如图所示,下列说法正确的是( )
在密闭容器中,1molH2与1molCO发生反应:CO(g)+2H2(g)?CH3OH(g),△H<0,反应达到平衡时,改变温度(T)和压强(P),反应混合物中甲醇的物质的量分数变化情况如图所示,下列说法正确的是( )| A. | P1<P2<P3<P4 | |
| B. | T1<T2<T3<T4 | |
| C. | T4和P1状态下,H2的平衡转化率为8/9 | |
| D. | 甲醇的物质的量分数越小,反应的平衡常数越小 |
13.新型纳米材料MFe2Ox(3<x<4)中M表示+2价的金属元素,在反应中M化合价不发生变化.常温下,MFe2Ox能使工业废气中的(SO2)转化为S,流程如下:MFe2Ox$→_{常温}^{SO_{2}}$MFe2Oy下列判断正确的是( )
| A. | SO2是该反应的催化剂 | B. | MFe2Ox是还原剂 | ||
| C. | X<Y | D. | SO2发生了置换反应 |
20.近年来,乳酸成为研究热点之一,以乳酸为原料制成的高分子材料具有生物兼容性.已知乳酸的结构简式为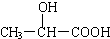 ,下列物质中能与乳酸反应的是( )
,下列物质中能与乳酸反应的是( )
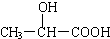 ,下列物质中能与乳酸反应的是( )
,下列物质中能与乳酸反应的是( )| A. | 金属铁 | B. | NH4Cl溶液 | C. | 乙烷 | D. | 苯 |
12.下列说法不正确的是( )
| A. | 石油主要成分都是碳氢化合物 | |
| B. | 煤经气化和液化两个物理变化过程,可变为清洁能源 | |
| C. | 天然气和沼气的主要成分是甲烷 | |
| D. | 75%(体积分数)的乙醇溶液常用于医疗消毒 |