题目内容
决定物质性质的重要因素是物质的结构。请回答下列问题:
(1)N、O、S三种元素的第一电离能从大到小的顺序为 。
(2)甲醛(H2C=O)分子碳原子的杂化方式为 用价层电子对互斥理论推断甲醛中H—C—H的键角 120o(填“>”“<”或“=”)。
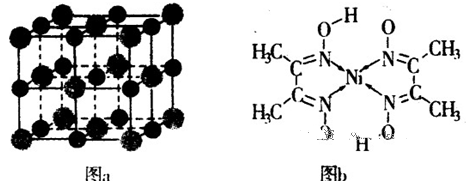
(3)科学家通过X射线探明,KCl、MgO、CaO的晶体结构与NaCl的晶体结构相似(图a所示)。KCl、CaO、MgO三种离子晶体熔点从高到低的顺序是 。
(4)设MgO晶胞的边长为acm,则MgO的密度是 g·cm-3(只要求列算式。阿伏加德罗常数为NA)。
(5)某配合物的分子结构如图b所示,其分子内不含有 (填字母)。
(1)N、O、S三种元素的第一电离能从大到小的顺序为 。
(2)甲醛(H2C=O)分子碳原子的杂化方式为 用价层电子对互斥理论推断甲醛中H—C—H的键角 120o(填“>”“<”或“=”)。
(3)科学家通过X射线探明,KCl、MgO、CaO的晶体结构与NaCl的晶体结构相似(图a所示)。KCl、CaO、MgO三种离子晶体熔点从高到低的顺序是 。
(4)设MgO晶胞的边长为acm,则MgO的密度是 g·cm-3(只要求列算式。阿伏加德罗常数为NA)。
(5)某配合物的分子结构如图b所示,其分子内不含有 (填字母)。
| A.离子键 | B.共价键 | C.金属键 | D.配位键 E.氢键 F.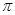 键 键 |

(1)N>O>S;(2)sp2;<;(3)MgO>CaO>KCl;(4)160/a3NA;(5)AC。
试题分析:(1)根据同周期同主族元素性质递变规律判断,同一周期由左向右元素原子的第一电离能呈递增趋势,但氮原子2p轨道为半充满状态,第一电离能比相邻的元素都大;同主族由上到下元素原子的第一电离能逐渐减小,N、O、S三种元素的第一电离能从大到小的顺序为N>O>S;(2)甲醛(H2C=O)分子碳原子的杂化方式为sp2;甲醛(H2C=O)分子中氧原子上含有两对孤对电子,对成键电子对有排斥作用,甲醛中H—C—H的键角<120o;(3)对于结构相似的离子晶体,晶格能越大晶体的熔点越高;晶格能的高低取决于离子半径和离子所带的电荷,离子半径越小,所带电荷越多,晶格能越大,熔点越高;则KCl、CaO、MgO三种离子晶体熔点从高到低的顺序是MgO>CaO>KCl;(4)根据MgO晶胞结构利用切割法分析知,1mol晶胞中含有4molMgO,质量为160g,晶胞的边长为acm,则1mol晶胞的体积为a3NAcm3则MgO的密度是160/a3NAg·cm-3;(5)根据配合物的分子结构判断,其分子内不含有离子键和金属键,选AC。

练习册系列答案
相关题目
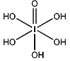 )和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6_____HIO4。(填“>”、“<”或“=”)
)和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6_____HIO4。(填“>”、“<”或“=”)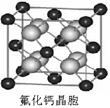


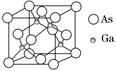
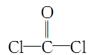 ,每个COCl2分子内含有________个σ键,________个π键,其中心原子采取________杂化轨道方式。
,每个COCl2分子内含有________个σ键,________个π键,其中心原子采取________杂化轨道方式。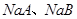 溶液的pH均大于7
溶液的pH均大于7