题目内容
2.单斜硫和正交硫转化为二氧化硫的能量变化如图所示,下列说法不正确的是( )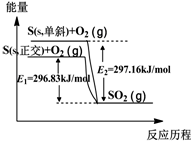
| A. | 单斜硫和正交硫互为同素异形体 | |
| B. | 正交硫比单斜硫稳定 | |
| C. | 相同物质的量的正交硫比单斜硫所含有的能量高 | |
| D. | 由单斜硫制取正交硫是一个放热反应 |
分析 由图象可以看出,单斜硫的能量比正交硫的能量高,物质的能量越高越不稳定,故单斜硫制取正交硫为放热反应,以此解答该题.
解答 解:A、由同种元素形成的不同单质互称同素异形体,单斜硫和正交硫是由同种元素形成的不同单质,故互为同素异形体,故A正确;
B、由图象可以看出,单斜硫的能量比正交硫的能量高,而物质的能量越高越不稳定,故正交硫比单斜硫稳定,故B正确;
C、由图象可以看出,相同物质的量的单斜硫的能量比正交硫的能量高,故C错误;
D、由于相同物质的量的单斜硫的能量比正交硫的能量高,故由单斜硫制取正交硫是一个放热反应,故D正确.
故选C.
点评 本题考查化学反应与能量的变化,题目难度不大,注意分析能量曲线,判断反应热、活化能与键能的关系.

练习册系列答案
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
12.如图是氢氧燃料电池(电解质为KOH)构造示意图.关于该电池的说法不正确的是( )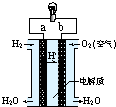

| A. | 电子由b通过灯泡流向a | |
| B. | 氢氧燃料电池是环保电池 | |
| C. | a极是负极 | |
| D. | 正极的电极反应是:O2+2H2O+4e-=4OH- |
10.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 用含0.1mol FeCl3的溶液与足量沸水反应制得的Fe(OH)3胶体中胶粒数为0.1NA | |
| B. | 0.1mol Fe 与0.1mol Cl2充分反应,转移的电子数为0.3 NA | |
| C. | 46g NO2和N2O4的混合气体中含N原子总数为NA | |
| D. | 等物质的量的NH4+和OH-含电子数均为10NA |
17.某有机物X(C4H6O5)广泛存在于许多水果内,该化合物具有如下性质:
①1molX与足量金属钠反应产生1.5mol气体;
②在有浓H2SO4和加热条件下,X与醇或羧酸均反应生成有香味的产物;
③X在一定条件下的分子内脱水产物(不是环状化合物)可和溴水发生加成反应.
根据上述信息,对X的结构判断正确的是( )
①1molX与足量金属钠反应产生1.5mol气体;
②在有浓H2SO4和加热条件下,X与醇或羧酸均反应生成有香味的产物;
③X在一定条件下的分子内脱水产物(不是环状化合物)可和溴水发生加成反应.
根据上述信息,对X的结构判断正确的是( )
| A. | X中含有碳碳双键 | B. | X中含有一个羧基和两个羟基 | ||
| C. | X中含有两个羧基和一个羟基 | D. | X中含有三个羟基和一个-COOR |
14.如图是产生和收集气体的实验装置,该装置适合于( )


| A. | 用浓硝酸与Cu反应制取NO2 | B. | 用浓盐酸和MnO2反应制取Cl2 | ||
| C. | 用H2O2溶液和MnO2反应制取O2 | D. | 用NH4Cl和Ca(OH)2反应制取NH3 |
11.在2L密闭容器中加入4molA和6molB,发生以下反应:4A(g)+6B(g)?4C(g)+5D(g).若经5s后,剩下的A是2.5mol,则A的反应速率是( )
| A. | 0.45 mol/(L•s) | B. | 0.15 mol/(L•s) | C. | 0.225 mol/(L•s) | D. | 0.9 mol/(L•s) |
12.中学常见物质A、B、C、D、E、X,存在图中转化关系(部分生成物和反应条件略去).下列推断不正确的是( )


| A. | 若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是氯气 | |
| B. | 若D是一种强碱,则A、B、C均可与X反应生成D | |
| C. | 若D为NaCl,且A可与C反应生成B,则E一定是CO2 | |
| D. | 若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C |
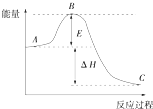 2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示,已知1mol SO2(g) 被氧化为1mol SO3(g)的△H=-99kJ/mol.回答下列问题:
2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示,已知1mol SO2(g) 被氧化为1mol SO3(g)的△H=-99kJ/mol.回答下列问题: .
. .肼-空气燃料电池是一种环保碱性燃料电池,其电解质溶液是20%-30%的KOH溶液.该燃料电池的正极的电极反应式是O2+2H2O+4e-═4OH-.
.肼-空气燃料电池是一种环保碱性燃料电池,其电解质溶液是20%-30%的KOH溶液.该燃料电池的正极的电极反应式是O2+2H2O+4e-═4OH-.