题目内容
【题目】实验室用 63%的浓HNO3(其密度为1.4g/mL)配制240mL0.50mol/L稀HNO3,若实验仪器有:A.10mL量筒 B.50mL量筒 C.托盘天平 D.玻璃棒 E.100mL容量瓶 F.250mL容量瓶 G.500mL容量瓶 H.胶头滴管 I.200mL烧杯
(1)此浓硝酸的物质的量浓度为_______mol/L。
(2)应量取63%的浓硝酸____mL,应选用____ (填仪器的字母编号)。
(3)实验时还需选用的仪器有D、I、______(填序号)。
(4)配制过程中,下列操作会使配制的稀硝酸溶液浓度偏高的是(填序号)_____。
①量取浓硝酸的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③溶解后未经冷却就移液
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
(5)容避瓶足专门用来配制一定体积一定浓度的溶液的仪器,以下有关容量瓶的叙述正确的有__________。
A.容量瓶上标有压强、温度、刻线
B.容量瓶不能长时间贮存试剂
C.为使实验更准确,容量瓶洗净后最好用欲配制的溶液润洗
D.用容量瓶配制溶液,容量瓶必须是干燥的
【答案】 14.0 8.9 A F、H ①③ B
【解析】(1)由公式C=![]() ,则浓硝酸的物质的量浓度为:C(HNO3)=
,则浓硝酸的物质的量浓度为:C(HNO3)= 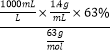 = 14.0mol/L。
= 14.0mol/L。
(2)、因无240mL的容量瓶,则根据容量瓶的规格,应配制250mL0.50mol/L稀HNO3,根据溶液稀释定律,C(浓硝酸)×V(浓硝酸)= C(稀硝酸)×V(稀硝酸),则V(浓硝酸)= 0.25L×0.50mol/L÷14.0 mol/L= 0.0089L,即8.9mL;为了减小称量误差,根据“大而近”的原则,应选择10mL的量筒。
(3)、根据溶液配制的步骤,此时还缺少250mL的容量瓶和胶头滴管,所以选F、H。
(4)、①.量取浓硝酸的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶中,会造成溶质的物质的量偏高,则物质的量浓度偏高,所以①正确;
②. 容量瓶使用时未干燥,因后续还要加水定容,所以对配制溶液无影响,②错误;
③. 溶解后未经冷却就移液,则冷却至室温时溶液体积会减小,则配制的溶液浓度偏高,所以③正确;
④. 定容时不小心有少量蒸馏水滴到瓶外,因损失的是蒸馏水,而不是溶质,根据定容的原则,可以继续加水至刻度线,所以对配制溶液的浓度无影响,所以④错误;
⑤.因为是定容以后振荡摇匀,静置,此时发现液面低于刻度线,是因为有部分溶液可能在瓶塞和瓶口结合处未能滴下,这属于正常情况,此时再加水会导致溶剂偏多,配制的溶液浓度偏低,故⑤错误。
所以此题答案为①③
(5)容量瓶上标有容积、温度和刻度线三种标识,没有压强,所以A错误;B项正确;用欲配制的溶液对容量瓶进行润洗,会造成所配制的溶液浓度偏高,故C错误;因容量瓶中含有少量水,对所配制的溶液无影响,所以D错误;此题答案为B


