题目内容
【题目】请阅读下列材料,完成下面小题。
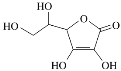
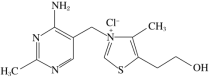
利用Kolbe's电解法制取乙炔的反应原理为: +2H2O
+2H2O 2CO2↑+C2H2↑+H2↑+2KOH
2CO2↑+C2H2↑+H2↑+2KOH
【1】下列表示反应中相关微粒的化学用语错误的是( )
A.中子数为20的钾原子:![]() K
K
B.K+的结构示意图:
C.CO2的电子式:![]()
D.C2H2的结构式:H—C![]() C—H
C—H
【2】有关该反应的下列说法正确的是( )
A.化学能转变为电能
B.电解槽中向阴极迁移的主要是H+
C.电解过程中溶液pH不断减小
D.阴极的电极反应式为2H2O+2e-=2OH-+H2↑
【3】下列羧酸钾盐中,其水溶液电解生成的烃主要是CH2=CH2的是( )
A.CH3COOKB.CH3CH2COOKC.CH2=CHCOOKD.KOOCCH2CH2COOK
【答案】
【1】C
【2】D
【3】D
【解析】
【1】
A.该K的核素中子数为20,质子数为19,故可表示为![]() K,A正确;
K,A正确;
B.K外层共19个电子,K+失去最外层电子,结构示意图为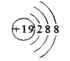 ,B正确;
,B正确;
C.CO2中C与O之间共用两对电子,电子式为![]() ,C错误;
,C错误;
D.C2H2中C与H之间为单键,C与C之间为三键,结构式为H—C![]() C—H,D正确;
C—H,D正确;
故选C。
【2】
A.该反应是电解反应,是电能转化为化学能,A错误;
B.根据电解反应,电解生成KOH,因此溶液中不会大量存在H+,B错误;
C.电解生成KOH,因此溶液的pH不断增大,C错误;
D.阴极区H2O放电,因此电极反应为2H2O+2e-=2OH-+H2↑,D正确;
故选D。
【3】
根据题目中制乙炔的反应,要生成一个不饱和键需要脱去两个羧酸钾,要制得CH2=CH2,需要有两个羧酸钾,且C和C之间以单键相连,故选D。

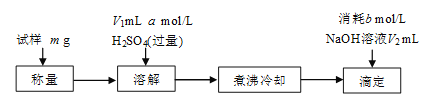
【题目】用含有A12O3、SiO2和少量FeO·xFe2O3的铝灰制备A12(SO4)3·18H2O。工艺流程如下:
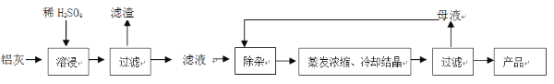
(一定条件下,![]() 可与Mn2+反应生成MnO2)
可与Mn2+反应生成MnO2)
已知: 生成氢氧化物沉淀的pH
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀时 | 3.4 | 6.3 | 2.7 |
完全沉淀时 | 5.2 | 9.7 | 3.2 |
(1)H2SO4溶解A12O3的离子方程式是_______________;
(2)检验滤液中还存在Fe2+的方法是____________(注明试剂、现象)。
(3)“除杂”环节有如下几个步骤:
(Ⅰ)向滤液中加入过量KMnO4溶液,调节溶液的pH为3.2;
(Ⅱ)加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
(Ⅲ)加入MnSO4至紫红色消失,过滤。
①步骤Ⅰ的目的_________;调节溶液的pH为3.2的目的是__________。
②向Ⅱ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是______,写出其反应方程式________________;
③Ⅲ中加入MnSO4的目的是__________。
(4)从多次循环使用后母液中可回收的主要物质是_________(填化学式)。
【题目】根据下列事实得出的结论正确的是( )。
选项 | 事实 | 结论 |
A | 甲、乙两种有机物具有相同的相对分子质量和不同的结构 | 甲和乙一定互为同分异构体 |
B | 质量相同的甲、乙两种有机物完全燃烧时产生质量相同的水 | 甲、乙两种分子中, |
C | 在淀粉溶液中加入稀硫酸,水浴加热一段时间后取出部分水解液,滴加银氨溶液后再加热,无银镜出现 | 淀粉的水解产物不具有还原性 |
D | 不存在两种邻二甲苯 | 苯分子中的碳碳键完全相同,苯不是单双键交替结构 |
A.AB.BC.CD.D
【题目】以CuSO4溶液和不同酸根离子形成的钠盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样性。
实验 | 试剂 | 现象 | |
| 滴管 | 试管 | |
0.2molL-1 CuSO4溶液 | 0.2molL-1NaI溶液 | Ⅰ.产生白色沉淀和黄色溶液 | |
0.2molL-1Na2CO3溶液 | Ⅱ.产生绿色沉淀和无色无味气体 | ||
0.2molL-1Na2SO3溶液 | Ⅲ.产生棕黄色沉淀 | ||
(1)经检验,现象Ⅰ的白色沉淀为CuI,则反应的离子方程式为___,氧化产物与还原产物的物质的量之比为___。
(2)经检验,现象Ⅱ中产生的气体是二氧化碳,绿色沉淀是碱式碳酸铜[xCuCO3yCu(OH)2zH2O]。现采用氢气还原法测定碱式碳酸铜组成,请回答如下问题:
①写出xCuCO3yCu(OH)2zH2O与氢气反应的化学方程式___;
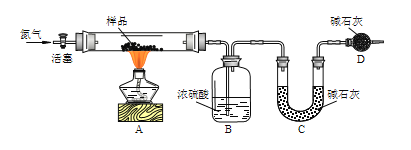
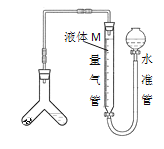
②实验装置用下列所有仪器连接而成,按氢气流方向的连接顺序是(填仪器接口字母编号):a→___→gf→___→___→___→l

(3)经检验,现象Ⅲ的棕黄色沉淀中不含SO42-,含有Cu+、Cu2+和SO32-。已知:Cu+![]() Cu+Cu2+
Cu+Cu2+
①用稀硫酸证实沉淀中含有Cu+的实验现象是___。
②通过下列实验证实,沉淀中含有Cu2+和SO32-。

a.白色沉淀A是BaSO4,试剂Ⅰ是___。
b.证实沉淀中含有Cu2+和SO32-的理由是___。