题目内容
13.重铬酸钾是工业生产和实验室的重要氧化剂,重铬酸钾的溶解度随温度影响较大.工业上常用铬铁矿(主要成分为FeO•Cr2O3,杂质为SiO2、Al2O3)为原料生产它,实验室模拟工业法用铬铁矿制K2Cr2O7的主要工艺如图.涉及的主要反应是:6FeO•Cr2O3+24NaOH+7KClO3=12Na2CrO4+3Fe2O3+7KCl+12H2O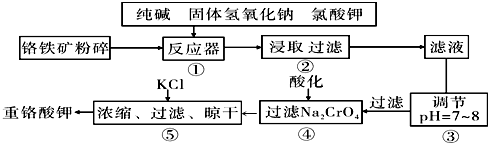
(1)碱浸前将铬铁矿粉碎的作用是增大接触面积,增大反应速率.
(2)步骤③调节pH后过滤得到的滤渣是H2SiO3、Al(OH)3.
(3)操作④中,酸化时,CrO${\;}_{4}^{2-}$转化为Cr2O${\;}_{7}^{2-}$,写出平衡转化的离子方程式2CrO42-+2H+?Cr2O72-+H2O.
(4)用简要的文字说明操作⑤加入KC1的原因温度对氯化钠的溶解度影响小,但对重铬酸钾的溶解度影响较大,利用复分解反应,可得到重铬酸钾.
(5)称取重铬酸钾试样2.500g配成250mL溶液,取出25mL于锥形瓶中,加入10mL 2mol/LH2SO4和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min.然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol/LNa2S2O3标准溶液滴定(I2+2S2O${\;}_{3}^{2-}$=2I-十S4O${\;}_{5}^{2-}$)判断达到滴定终点的依据是当滴加最后一滴硫代硫酸钠溶液时,溶液蓝色褪去,半分钟内不变色.
分析 流程分析可知,铬铁矿(主要成分为FeO•Cr2O3,杂质为SiO2、Al2O3)为原料粉碎后再反应器中加入纯碱、固体氢氧化钠、氯酸钾浸取过滤得到滤液调节溶液PH除去铝和硅酸根离子,过滤得到Na2CrO4溶液,酸化后加入氯化钾浓缩过滤干燥得到重铬酸钾;
(1)依据影响化学反应速率的因素分析,增大接触面积会加快反应速率;
(2)根据水解平衡移动判断产物;
(3)在酸性环境下,CrO42-转化为Cr2O72-,据此来书写方程式;
(4)操作⑤加入KCl的原因温度对氯化钠的溶解度影响小,但对重铬酸钾的溶解度影响较大;
(5)根据反应:I2+2S2O32-=2I-+S4O62-,碘单质遇到淀粉时,溶液的蓝色消失,据此来回答.
解答 解:(1)碱浸前将铭铁矿粉碎的作用是增大接触面积加快反应速率,
故答案为:增大接触面积,增大反应速率;
(2)由于硅酸钠和偏铝酸钠在溶液中发生水解,SiO32-+H2O?HSiO3-+OH-、HSiO3-+H2O?H2SiO3+OH-、AlO2-+2H2O?Al(OH)3+OH-,降低pH有利于水解平衡向正反应方向移动,当pH调到7~8时能使它们完全水解生成沉淀,
故答案为:H2SiO3、Al(OH)3;
(3)在酸性环境下,CrO42-转化为Cr2O72-,即2CrO42-+2H+?Cr2O72-+H2O,
故答案为:2CrO42-+2H+?Cr2O72-+H2O;
(4)操作⑤加入KCl的原因温度对氯化钠的溶解度影响小,但对重铬酸钾的溶解度影响较大,利用复分解反应,可得到重铬酸钾;
故答案为:温度对氯化钠的溶解度影响小,但对重铬酸钾的溶解度影响较大,利用复分解反应,可得到重铬酸钾;
(5)根据反应:I2+2S2O32-=2I-+S4O62-,当滴加最后一滴硫代硫酸钠溶液时,碘单质恰好完全反应,溶液蓝色褪去,达到滴定终点,
故答案为:当滴加最后一滴硫代硫酸钠溶液时,溶液蓝色褪去,半分钟内不变色.
点评 本题考查较为综合,涉及氧化还原反应、溶解平衡以及滴定操作等问题,题目难度中等,本题注意从质量守恒的角度利用关系式法计算.

 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案| A. | 2LCO和2L CO2 | |
| B. | 9克H2O和标准状况下11.2L CO2 | |
| C. | 标准状况下1mol O2和22.4L H2O | |
| D. | 0.2mol H2和标准状况下4.48L HCl气体 |
| A. | 标准状况下,2.24 L HF含有的HF分子数为0.1NA | |
| B. | 在常温常压下,32 g 18O2中含有2NA氧原子 | |
| C. | 25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| D. | 1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,转移的电子数为NA |
| A. | 0.1mol钠离子含有电子数为1.1NA | |
| B. | 在常温常压下,1mol氩气含有的原子数为2NA | |
| C. | 1molNa2O2中含有离子数为3NA | |
| D. | 1molCCl2F2中含有氯气分子数为NA |
| A. | 原子半径由大到小的顺序:W>Z>Y>X,简单离子半径由大到小的顺序:X>Y>Z | |
| B. | 原子最外层电子数由多到少的顺序:Y>X>W>Z,最高正价由高到低顺序:W>Z | |
| C. | 元素非金属性由强到弱的顺序:Z>W>X,W的单质常温下可与氢氧化钠溶液反应 | |
| D. | 简单气态氢化物的稳定性由强到弱的顺序:X>Y>W |
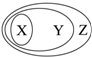 如图从属关系中错误的是( )
如图从属关系中错误的是( )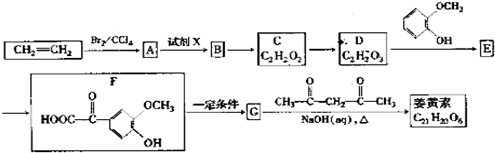

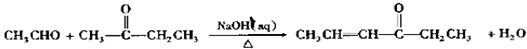

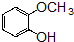 +OHCCOOH→
+OHCCOOH→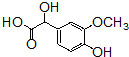 ,其反应类型是加成反应.
,其反应类型是加成反应.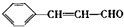 ),写出制备肉桂醛所需有机物的结构简式C6H5CHO、CH3CHO.
),写出制备肉桂醛所需有机物的结构简式C6H5CHO、CH3CHO.