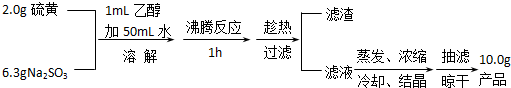
题目内容
20.下列实验操作中正确的是( )| A. | 用浓硫酸配制稀硫酸时,浓硫酸缓慢加入水中,并用玻璃棒不断搅拌 | |
| B. | 用酒精和汽油都可以萃取碘水中的碘 | |
| C. | 潮湿的或具有腐蚀性的药品,必须放在玻璃器皿里称量,其他固体药品可直接放在天平托盘上称量 | |
| D. | 用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 |
分析 A.稀释浓硫酸,将密度大的液体注入密度小的液体中;
B.酒精与水以任意比例互溶;
C.固体药品不能直接放在天平托盘上称量,需要垫一张大小相同的纸片进行称量;
D.过量的试剂不能倒回试剂瓶中,防止污染试剂.
解答 解:A.稀释浓硫酸,将密度大的液体注入密度小的液体中,且稀释放热,则在烧杯中加水,沿着烧杯内壁缓慢加入浓硫酸,并用玻璃棒不断搅拌,防止液滴飞溅,故A正确;
B.酒精与水以任意比例互溶,不能提取碘水中的碘,故B错误;
C.潮湿或具有腐蚀性的药品,必须放在玻璃器皿里称量,但是其他固体药品不能直接放在天平托盘上称量,需要垫一张大小相同的纸片进行称量,故C错误;
D.过量的试剂不能倒回试剂瓶中,防止污染试剂,应放在指定的烧杯中,故D错误.
故选A.
点评 本题考查化学实验方案的评价,为高频考点,涉及萃取、称量、稀释等实验基本操作,侧重实验基本技能和基础知识的考查,注意实验操作的评价性、操作性分析,题目难度不大.

练习册系列答案
相关题目
10.某溶液中大量存在的五种离子:Cl-、SO42-、Al3+、H+、M,其物质的量之比为:n(Cl-):n(SO42-):n(Al3+):n(H+):n(M)=2:3:1:3:2,则M可能为( )
| A. | Mg2+ | B. | Na+ | C. | CO32- | D. | Ba2+ |
11.下列说法不正确的是( )
| A. | 医用酒精的浓度通常为75% | |
| B. | 用灼烧并闻气味的方法区别纯棉织物和纯毛织物 | |
| C. | 采集某雨水样品,放置一段时间,pH由4.8变为4.2,是因为水中溶解了较多的CO2 | |
| D. | 单质硅是将太阳能转变为电能的常用材料 |
5.下列说法正确的是( )
| A. | 煤的气化、液化是物理变化,煤的干馏是化学变化 | |
| B. | C60、液氯是单质,HD、干冰是化合物,NO2是酸性氧化物 | |
| C. | 烟、雾属于胶体,能产生丁达尔效应 | |
| D. | 可用热的饱和碳酸钠溶液除去金属表面的石蜡 |
12.下列说法正确的是( )
| A. | SO2属于酸性氧化物,CaO属于碱性氧化物 | |
| B. | 盐酸,硝酸都属于无氧酸 | |
| C. | 氢氧化钠,氢氧化铁都是可溶性碱 | |
| D. | CO,CO2都是酸性氧化物 |
9.下列各组中的两稀溶液间的反应,可以用同一个离子方程式来表示的是( )
| A. | HCl与Na2CO3;HNO3与KHCO3 | B. | BaCl2与Na2SO4;Ba(OH)2与CuSO4 | ||
| C. | HCl与KOH;H2SO4与Ba(OH)2 | D. | H2SO4与NaHCO3;NaHSO4与KHCO3 |
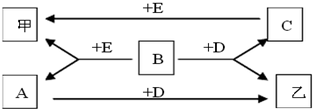 已知甲、乙两种白色固体都不溶于水不溶于稀硝酸,A、B、C、D、E 均是能溶于水的化合物.
已知甲、乙两种白色固体都不溶于水不溶于稀硝酸,A、B、C、D、E 均是能溶于水的化合物.