题目内容
8.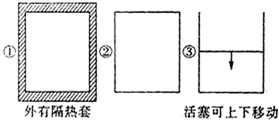 在如图所示的容积相同的三个容器①②③中进行如下反应:3A(g)+B(g)?2C(g)△H<0,若起始温度相同,分别向三个容器中充入6mol A和2mol B,则达到平衡时各容器中C物质的百分含量由大到小的顺序为③②①(填容器编号).
在如图所示的容积相同的三个容器①②③中进行如下反应:3A(g)+B(g)?2C(g)△H<0,若起始温度相同,分别向三个容器中充入6mol A和2mol B,则达到平衡时各容器中C物质的百分含量由大到小的顺序为③②①(填容器编号).
分析 ①容器是绝热恒容容器,反应进行过程中是放热反应,温度升高;
②是恒温恒容容器,反应进行过程中反应放热,热量散发,压强减小;
③是恒温恒压容器,反应进行过程中保持恒压.
解答 解:①容器是绝热恒容容器,反应进行过程中是放热反应,温度升高;
②是恒温恒容容器,反应进行过程中反应放热,热量散发,压强减小;
③是恒温恒压容器,反应进行过程中保持恒压;
①与②相比,由于②能把反应产生的热量散到空中,相比①来说相当于降低温度,故平衡右移,故平衡时C的体积分数②大于①;②与③相比,由于反应向右移进行时分子数减少,故③中活塞下移,相对②来说,相当于给体系加压,平衡右移,故B、C的体积分数③大于②,达到平衡时各容器中C物质的体积分数由大到小的顺序为③②①,故答案为:③②①.
点评 本题考查了本题容器的特征分析判断,化学平衡移动原理,改变平衡移动方向的分析是解题关键,题目难度中等.

练习册系列答案
相关题目
16.在一固定体积的密闭容器中,进行着下列化学反应:CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
则下列有关的叙述正确的是( )
| T(℃) | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
| A. | 该反应为放热反应 | |
| B. | 可测量容器总压变化来判定化学反应是否达到平衡 | |
| C. | 若在某平衡状态时,c(CO2)×c(H2)=c(CO)×c(H2O),此时的温度为830℃ | |
| D. | 达平衡时,浓度:c(CO2)=c(CO) |
18.今有7种物质:①铜 ②氯化氢 ③稀硫酸 ④氨气 ⑤碳酸钙 ⑥二氧化碳
将上述物质序号按要求填入下表.
将上述物质序号按要求填入下表.
| 序号 | 符合的条件 | 物质的序号 |
| 1 | 电解质,但熔融状态下并不导电 | |
| 2 | 电解质,但难溶于水 | |
| 3 | 非电解质 | |
| 4 | 既不是电解质,也不是非电解质,但本身能导电 |

 .
.