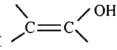题目内容
【题目】过氧乙酸(![]() ),是一种高效消毒剂,它可由冰醋酸和过氧化氢在浓硫酸催化作用下制得,实验装置和步骤如下
),是一种高效消毒剂,它可由冰醋酸和过氧化氢在浓硫酸催化作用下制得,实验装置和步骤如下
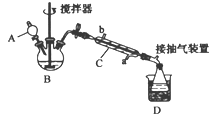
①在三颈烧瓶中加入一定量冰醋酸与浓硫酸的混合物,再缓缓加入适量30%的双氧水;
②不断搅拌并控制装置B中混合液的温度为20~30℃至反应结束;
③接入仪器C和抽气泵,在锥形瓶中收集得到产品。
回答下列问题:
(1)仪器C的名称是_______,仪器C中冷水流入口是_______ (填“a”或“b”)。
(2)为更好地控制反应温度,应采用的加热方法是______________。
(3)生成过氧乙酸的化学方程式为_________________。
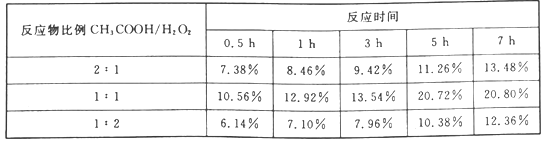
(4)实验测得产物过氧乙酸的百分含量随反应物比例和反应时间的变化数据如下表。由表中数据可知,反应物最佳比例(CH3COOH/H2O2)是_______,最佳反应时间约_______。
(5)产品中过氧乙酸浓度的测定:取2.00mL过氧乙酸产品试样,加水稀释成100mL;从中取出5.00mL,逐滴滴加酸性KMnO4溶液至溶液恰好呈粉红色,以除去残余的H2O2;再加入稍过量的KI溶液,发生反应CH3COOOH+2I-+2H+=I2+CH3COOH+H2O;反应完全后,滴入几滴淀粉溶液,用0.1000mol·L-1的Na2S2O3标准液滴定至终点(反应式为2S2O32-+I2=S4O62-+2I-),消耗14.30mLNa2S2O3标准液。则产品中过氧乙酸的物质的量浓度是________mol·L-1 (保留2位小数)。
【答案】直形冷凝管 a 水浴加热 ![]() 1:1 5h 7.15
1:1 5h 7.15
【解析】
(1)由仪器结构,可知C为直形冷凝管,采取逆流原理通入冷凝水;
(2)控制B中混合液的温度为20~30℃,应采取水浴加热;
(3)乙酸与过氧化氢在浓硫酸、20~30℃条件下反应生成CH3COOOH,乙酸羧基中H原子被过氧化氢的OH替代,同时生成H2O;
(4)生成的过氧乙酸含量越高越好,结合表格中数据选择;
(5)根据关系式:CH3COOOH~I2~2Na2S2O3,计算稀释后的5mL溶液中过氧乙酸的物质的量,进而计算原来的2mL溶液中过氧乙酸的物质的量,在根据物质的量浓度定义式计算。
(1)仪器C为冷凝管,冷凝水应当低进高出,则流入口为a,故答案为:冷凝管;a;
(2)为更好地控制反应温度,应采用的加热方法是水浴加热,故答案为:水浴加热;
(3)过氧乙酸由过氧化氢氧化乙酸得到,化学方程式为![]() ;
;
(4)分析图表可知,当反应物比例为1:1时,过氧乙酸的百分含量最高,且反应达到5h为最佳反应时间,故答案为1:1;5h;
(5)根据关系式:CH3COOOH~I2~2Na2S2O3,可知稀释后的5mL溶液中过氧乙酸的物质的量=![]() ×0.0143L×0.1000mol/L,原来的2mL溶液中过氧乙酸的物质的量=
×0.0143L×0.1000mol/L,原来的2mL溶液中过氧乙酸的物质的量=![]() ×0.0143L×0.1000mol/Lmol×
×0.0143L×0.1000mol/Lmol×![]() =0.0143mol,故该样品中过氧乙酸的物质的量浓度是
=0.0143mol,故该样品中过氧乙酸的物质的量浓度是![]() =7.15mol/L,故答案为:7.15。
=7.15mol/L,故答案为:7.15。