题目内容
酸碱中和滴定是利用中和反应,用已知浓度的酸(或碱)来测定未知浓度的碱(或酸)的实验方法,其中溶液的pH变化是判断滴定终点的依据。
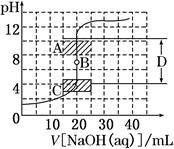
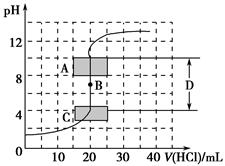
(1)为了准确绘制上图,在滴定开始时和________,滴液速度可以稍快一点,测试和记录pH的间隔可大些;当接近________时,滴液速度应该慢一些,尽量每滴一滴就测试一次。
(2)在图中A的pH范围使用的指示剂是____________;C的pH范围使用的指示剂是________________;D区域为________________。
(3)用0.1 032 mol·L-1的盐酸溶液滴定未知浓度的氢氧化钠溶液,重复三次的实验数据如下表所示:
则待测氢氧化钠的物质的量浓度是________mol·L-1。在上述滴定过程中,若滴定前滴定管下端尖嘴中有气泡,滴定后气泡消失,则测定结果将________(填“偏高”、“偏低”或“不影响”)。
(4)下列关于上述中和滴定过程中的操作正确的是________(填字母)。
A.用碱式滴定管量取未知浓度的烧碱溶液
B.滴定管和锥形瓶都必须用待盛放液润洗
C.滴定中始终注视锥形瓶中溶液颜色变化
D.锥形瓶中的待测液可用量简量取

(1)为了准确绘制上图,在滴定开始时和________,滴液速度可以稍快一点,测试和记录pH的间隔可大些;当接近________时,滴液速度应该慢一些,尽量每滴一滴就测试一次。
(2)在图中A的pH范围使用的指示剂是____________;C的pH范围使用的指示剂是________________;D区域为________________。
(3)用0.1 032 mol·L-1的盐酸溶液滴定未知浓度的氢氧化钠溶液,重复三次的实验数据如下表所示:
| 实验序号 | 消耗0.1 032 mol·L-1的盐酸溶液的体积/mL | 待测氢氧化钠溶液的体积/mL |
| 1 | 28.84 | 25.00 |
| 2 | 27.83 | 25.00 |
| 3 | 27.85 | 25.00 |
则待测氢氧化钠的物质的量浓度是________mol·L-1。在上述滴定过程中,若滴定前滴定管下端尖嘴中有气泡,滴定后气泡消失,则测定结果将________(填“偏高”、“偏低”或“不影响”)。
(4)下列关于上述中和滴定过程中的操作正确的是________(填字母)。
A.用碱式滴定管量取未知浓度的烧碱溶液
B.滴定管和锥形瓶都必须用待盛放液润洗
C.滴定中始终注视锥形瓶中溶液颜色变化
D.锥形瓶中的待测液可用量简量取
(1)滴定终点后 滴定终点 (2)酚酞 甲基橙 pH突变范围 (3)0.114 9 偏高 (4)AC
(1)由图像可知,天始时和结束时溶液pH变化都不大,所以可以快一点;而在滴定终点附近,溶液的pH变化非常快非常大,所以要慢一点。(2)A区域的pH范围内溶液显碱性,应选择酚酞等碱性范围内变色的指示剂;C区域的pH范围内溶液显酸性,应选择甲基橙等酸性范围内变色的指示剂。而D区域内消耗的试剂的体积很小,但是溶液pH变化非常大,是滴定终点前后pH的突变范围。(3)第一组数据明显偏大,超出误差允许范围,必须舍弃,所以25.00 mL氢氧化钠溶液平均消耗27.84 mL盐酸。c(NaOH)=27.84 mL×0.103 2 mol·L-1÷25.00 mL=0.114 9 mol·L-1。若滴定前滴定管下端尖嘴中有气泡,滴定后气泡消失,则测的盐酸体积增大,计算结果将偏高。(4)中和滴定是准确测定溶液浓度的方法,所量液体的体积都要准确,所以A正确、D错误。B项滴定管一定要润洗,否则所装液体会被稀释,浓度变小。锥形瓶一定不能润洗,否则锥形瓶中所装液体的物质的量会增大,测量结果不正确,错误。C项滴定过程中应该始终注视锥形瓶中溶液颜色变化,及时判断出滴定终点并关闭活塞,正确。

练习册系列答案
相关题目


 H++OH- ΔH=Q(Q>0)的平衡,下列叙述一定正确的是( )
H++OH- ΔH=Q(Q>0)的平衡,下列叙述一定正确的是( )