题目内容
8.下列有关说法中,不正确的是( )| A. | 维勒用无机物合成了尿素,突破了无机物和有机物的界限 | |
| B. | 石油裂解的目的是提高汽油等轻质油的产量和质量 | |
| C. | 羟基不带电,氢氧根带一个单位负电荷,氢氧根比羟基稳定 | |
| D. | 苯分子中不存在单双键交替的事实是苯的邻二取代物没有同分异构体 |
分析 A.1828年德国化学家维勒,将一种无机物NH4CNO的水溶液加热得到了有机物尿素;
B.石油裂解的主要目的是得到更多的乙烯、丙烯等气态短链烃;
C.羟基含有9个电子,氢氧根离子含有10个电子,羟基和氢氧根离子中都含有9个质子;
D.邻二溴苯仅有一种空间结构可证明苯分子中不存在单双键交替的结构.
解答 解:A.维勒将无机物NH4CNO在一定条件下合成尿素,尿素为有机物,故A正确;
B.石油裂解的目的是为了获得乙烯、丙烯、丁二烯、丁烯、乙炔等,故B错误;
C.羟基含有9个电子,氢氧根离子含有10个电子,羟基和氢氧根离子中都含有9个质子,所以羟基不带电,氢氧根带一个单位负电荷,氢氧根比羟基稳定,故C正确;
D.若苯的结构中存在单双键交替结构,苯的邻位二元取代物有两种,但实际上无同分异构体,所以能说明苯不是单双键交替结构,故D正确.
故选B.
点评 本题综合考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,有利于培养学生良好的科学素养,提高学生的积极性,难度不大.

练习册系列答案
相关题目
18.下列各组气态氢化物稳定性由强到弱的顺序排列的是( )
| A. | SiH4、PH3、H2S、HCl | B. | HF、HCl、HBr、HI | ||
| C. | PH3、H2S、HCl、HF | D. | NH3、PH3、AsH3、HF |
19.氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于区域3的( )
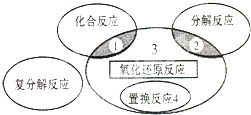

| A. | 4Fe(0H)2+O2+2H2O═4Fe(OH)3 | B. | 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2 O+CO2↑ | ||
| C. | 4NH3+5O2 $\frac{\underline{催化剂}}{△}$4NO+6H2O | D. | Zn+H2SO4═ZnSO4+H2↑ |
16.下列物质属于同分异构体的是( )
| A. | 葡萄糖与蔗糖 | B. | 蔗糖与麦芽糖 | C. | 动物油和脂肪 | D. | 淀粉和纤维素 |
20.下列有机物的命名正确的是( )
| A. | 2,4-二乙基戊烷 | B. | 4-甲基-3-乙基戊烷 | ||
| C. | 1,3,4-三甲苯 | D. | 2-甲基-2-氯丙烷 |
17.酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是有碳粉,二氧化锰,氯化锌和氯化铵等组成的填充物,该电池在放电过程产生MnOOH,回收处理该废电池可以得到多种化工原料,有关数据表所示:
溶解度/(g/100g水)
回答下列问题:
(1)该电池的负极为锌,正极反应式为MnO2+H++e-=MnOOH;
(2)维持电流强度为0.5A,电池工作5分钟,理论消耗Zn0.05gg;(已知F=96500C/mol)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有氯化锌和氯化铵,两者可以通过加热浓缩、冷却结晶分离回收,滤渣的主要成分是二氧化锰、碳粉和MnOOH,欲从中得到较纯的二氧化锰,最简便的方法是空气中加热,其原理是碳粉转变为二氧化碳,MnOOH氧化为二氧化锰;
(4)用废电池的锌皮制作七水合硫酸锌,需去除少量杂质铁,其方法是:加入稀硫酸和双氧水,溶解,铁变为Fe3+加碱调节PH为2.7,铁刚好完全沉淀(离子浓度≤1×10-5 mo1•L-1时即可认为离子沉淀完全)继续加碱调节PH为6锌开始沉淀(假定此时溶液中Zn2+的浓度为0.1mo1•L-1).若上述过程不加双氧水的后果Zn2+和Fe2+分离不开,原因是Fe(OH)2和Zn(OH)2的Ksp相近.
溶解度/(g/100g水)
温度/℃ 化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
| NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
(1)该电池的负极为锌,正极反应式为MnO2+H++e-=MnOOH;
(2)维持电流强度为0.5A,电池工作5分钟,理论消耗Zn0.05gg;(已知F=96500C/mol)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有氯化锌和氯化铵,两者可以通过加热浓缩、冷却结晶分离回收,滤渣的主要成分是二氧化锰、碳粉和MnOOH,欲从中得到较纯的二氧化锰,最简便的方法是空气中加热,其原理是碳粉转变为二氧化碳,MnOOH氧化为二氧化锰;
(4)用废电池的锌皮制作七水合硫酸锌,需去除少量杂质铁,其方法是:加入稀硫酸和双氧水,溶解,铁变为Fe3+加碱调节PH为2.7,铁刚好完全沉淀(离子浓度≤1×10-5 mo1•L-1时即可认为离子沉淀完全)继续加碱调节PH为6锌开始沉淀(假定此时溶液中Zn2+的浓度为0.1mo1•L-1).若上述过程不加双氧水的后果Zn2+和Fe2+分离不开,原因是Fe(OH)2和Zn(OH)2的Ksp相近.
 如图是一种形状酷似一条小狗的有机物.化学家Tim Rickard将其取名为“doggycene”.doggycene的分子式为C26H26.该分子中所有碳原子可能(填“可能”或“不可能”)处予同一平面.
如图是一种形状酷似一条小狗的有机物.化学家Tim Rickard将其取名为“doggycene”.doggycene的分子式为C26H26.该分子中所有碳原子可能(填“可能”或“不可能”)处予同一平面.