题目内容
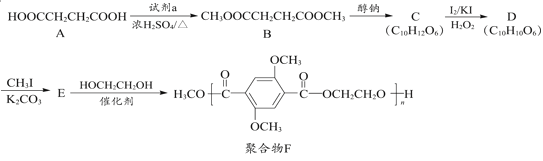
【题目】有机物A是一种重要的化工原料,用A制取新型聚合物F的合成路线如图:
已知:
ⅰ.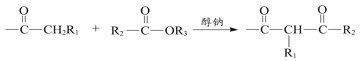 +R3OH
+R3OH
ⅱ.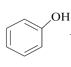 +R1I
+R1I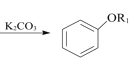 +HI
+HI
ⅲ.R1COOR2+R3OH![]() R1COOR3+R2OH
R1COOR3+R2OH
回答下列问题:
(1)A中官能团的结构简式为___。
(2)试剂a的名称___。1molD与足量的氢氧化钠溶液反应所需氢氧化钠的物质的量___。
(3)C中含有一个六元环,C的结构简式为___。
(4)C→D的反应类型为___。
(5)E→F的化学方程式是___。
(6)下列说法正确的是___(填序号)。
a.A能与NaHCO3溶液反应
b.醇钠可由醇与氢氧化钠反应制得
c.用FeCl3溶液不能鉴别D和E
d.HOCH2CH2OH俗称甘油
【答案】羧基 甲醇 4 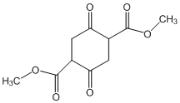 氧化反应
氧化反应 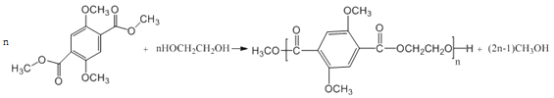 a
a
【解析】
比较B和A的结构简式可知,A发生酯化反应生成B,所以试剂a为CH3OH,根据C的化学式及B到C的条件可知,B发生信息i中的反应得C为: ,C发生氧化反应得D为
,C发生氧化反应得D为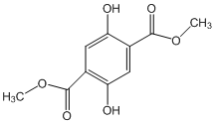 ,D发生信息ii中的反应生成E为
,D发生信息ii中的反应生成E为 ,E发生缩聚反应得F。
,E发生缩聚反应得F。
(1)根据A的结构简式可知,A中官能团的名称为羧基,故答案为:羧基;
(2)根据上面的分析可知,a为CH3OH,名称为甲醇;由分析可知D的结构为: ,能与NaOH溶液反应的官能团有酚羟基、酯基,1molD与足量的氢氧化钠溶液反应所需氢氧化钠的物质的量为4mol故答案为:甲醇;4;
,能与NaOH溶液反应的官能团有酚羟基、酯基,1molD与足量的氢氧化钠溶液反应所需氢氧化钠的物质的量为4mol故答案为:甲醇;4;
(3)根据上面的分析可知,C的结构简式为 ;
;
(4)C发生氧化反应得D,C→D的反应类型为氧化反应,故答案为:氧化反应;
(5)E发生缩聚反应得F,E→F的化学方程式是:
 ;
;
(6)a.A中含有羧基,A能与NaHCO3溶液反应,故a正确;
b.醇与金属钠反应得到醇钠和氢气,醇与NaOH不反应,故b错误;
c.D中有酚羟基,而E中没有,所以可用FeCl3溶液鉴别D和E,故c错误;
d.HOCH2CHOHCH2OH俗称甘油,故d错误,
故答案为:a。

 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
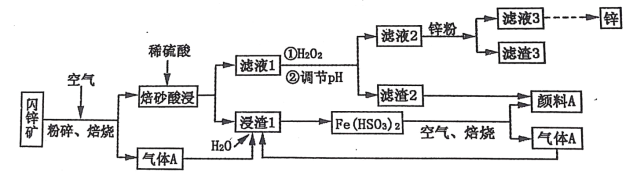
各地期末复习特训卷系列答案【题目】如图所示,某化学兴趣小组设计了一个燃料电池,并探究氯碱工业原理和粗铜精炼原理,其中乙装置中X为阳离子交换膜。根据要求回答相关问题:

(1)通入氧气的电极为_____(填“正极”或“负极”),通氢气一极的电极反应式为_________________;
(2)铁电极为_______(填“阳极”或“阴极”),乙装置中电解反应的化学方程式为_________________。
(3)若在标准状况下,有1.12 L氧气参加反应,丙装置中阴极增重的质量为______g;
(4)某粗铜中含有铁、金、银和铂等杂质,通过电解精制后,为从电解液中制得硫酸铜晶体(CuSO4·5H2O),设计了如下工艺流程:

已知:几种金属阳离子开始沉淀和沉淀完全的pH:
氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
Fe3+ | 1.9 | 3.2 |
Fe2+ | 7.0 | 9.0 |
Cu2+ | 4.7 | 6.7 |
①步骤I中加入试剂A的目的是_____________________________,试剂A应选择______(填序号);
a.氯气 b.过氧化氢 C.酸性高锰酸钾溶液
选择该试剂的原因_____________________________________________________;
②步骤II中试剂B为_________,调节pH的范围是___________;
③步骤III的操作是加热浓缩、_______、___________。
【题目】下列实验设计能达到相应实验目的是![]()
选项 | 实验设计 | 实验目的 |
A | 在热的NaOH溶液中滴入饱和 | 制备 |
B | 将 | 验证 |
C | 向含少量 | 除去 |
D | 将 | 比较 |
A.AB.BC.CD.D