题目内容
20.25℃时,水的电离达到平衡:H2O?H++OH-,△H>0,下列叙述正确的是( )| A. | 将水加热,Kw增大,pH不变 | |
| B. | 向水中加入稀氨水,平衡逆向移动,c(OH-)降低 | |
| C. | 向水中加入少量固体硫酸氢钠,溶液温度不变,则c(H+)增大,Kw不变 | |
| D. | 向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
分析 水电离生成氢离子、氢氧根离子,所以加入能电离出氢离子或氢氧根离子的物质抑制水电离,加入和氢离子或氢氧根离子反应的物质能促进水电离,温度不变,离子积常数不变,据此分析解答.
解答 解:A.水的电离是吸热过程,升高温度促进水电离,则Kw增大,pH减小,故A错误;
B.一水合氨电离出OH-而导致溶液中c(OH-)增大,从而抑制水电离,故B错误;
C.向水中加入硫酸氢钠固体,硫酸氢钠电离出氢离子导致溶液中c(H+)增大,温度不变Kw不变,故C正确;
D.水中加入醋酸钠,醋酸钠为强碱弱酸盐,醋酸根水解促进水的电离,平衡正向移动,故D错误,故选C.
点评 本题考查离子积常数、水的电离,明确氢离子或氢氧根离子抑制水电离、弱离子促进水电离即可解答,注意离子积常数与溶液酸碱性无关,置于温度有关,为易错点.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
16.下列变化中,一定伴随着化学变化的是( )
| A. | 加热碘,收集到紫黑色固体 | |
| B. | 将NaCl固体溶于水后离子键被破坏 | |
| C. | 将CCl4加入溴水中,观察到CCl4成橙色 | |
| D. | 将H2O2滴加在MnO2中,可收集到无色气体 |
15.下列各组物质中,符合前者为混合物,后者为单质的是( )
| A. | Na2CO3•10H2O Na2CO3 | B. | 冰水混合物 液氮 | ||
| C. | 石油 液氢 | D. | 碘酒 干冰 |
5.可用于干燥NH3的试剂是( )
| A. | 无水CaCl2 | B. | 浓H2SO4 | C. | P2O5 | D. | 碱石灰 |
12.对室温下c(H+)相同、体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是( )
| A. | 加适量的醋酸钠晶体后,两溶液的c(H+)均减小 | |
| B. | 使温度都升高20℃后,两溶液的c(H+)均不变 | |
| C. | 加水稀释2倍后,两溶液的c(H+)均增大 | |
| D. | 加足量的锌充分反应后,两溶液中产生的氢气一样多 |
9.将质量相等的下列各物质完全酯化时,需醋酸质量最多的是( )
| A. | 甲醇 | B. | 乙二醇 | C. | 丙醇 | D. | 甘油 |
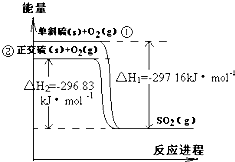 单斜硫和正交硫转化为二氧化硫的能量变化图如图,回答下列问题:
单斜硫和正交硫转化为二氧化硫的能量变化图如图,回答下列问题: