题目内容
【题目】实验室用下图所示装置制备干燥纯净的氯气,并进行氯气的性质实验。请回答下列问题:
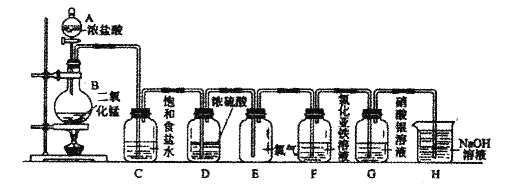
(1)A中盛有浓盐酸,B中盛有MnO2,则烧瓶中发生反应的化学方程式为:
_________________________________________________________
(2)C中盛有饱和食盐水,其作用是________________________________,D中浓硫酸的作用是___________________________________。
(3)F中是FeCl2溶液,F中发生反应的离子方程式为___________________
(4)G中是AgNO溶液,现象是______________________________
(5)H中盛有Na0H溶液,其作用是_____________________________。
【答案】MnO2+ 4HCl(浓)![]() MnCl2+ Cl2↑ + 2H2O 除去氯气中的HCl 干燥氯气(或吸收水分) Cl2+2Fe2+= 2Cl—+ 2Fe3+ 溶液中出现白色浑浊 吸收氯气,防止污染
MnCl2+ Cl2↑ + 2H2O 除去氯气中的HCl 干燥氯气(或吸收水分) Cl2+2Fe2+= 2Cl—+ 2Fe3+ 溶液中出现白色浑浊 吸收氯气,防止污染
【解析】
(1)二氧化锰与浓盐酸加热生成氯化锰、氯气和水,反应的化学方程式为:MnO2+ 4HCl(浓)![]() MnCl2+ Cl2↑ + 2H2O;
MnCl2+ Cl2↑ + 2H2O;
(2)用二氧化锰和浓盐酸共热制得的氯气中混有HCl和H2O(g);氯化氢极易溶于水,氯气能溶于水,且与水反应,Cl2+H2O=H++Cl﹣+HClO,食盐水溶液中的氯离子抑制氯气的溶解,降低氯气的溶解度,用饱和食盐水除去氯气中的HCl;浓硫酸有吸水性,且不和氯气反应,所以可用浓硫酸干燥氯气,
故答案为除去挥发出的HCl气体;干燥氯气;
(3)氯气与氯化亚铁反应生成氯化铁,离子方程式为:Cl2+2Fe2+=2Cl﹣+2Fe3+;
(4)氯水中含有氯离子,氯离子与硝酸银反应生成白色的氯化银沉淀,故答案为溶液中出现白色浑浊;
(5)氯气有毒,污染环境,所以不能直接排空;氯气能和氢氧化钠反应生成氯化钠、次氯酸钠和水,所以可用氢氧化钠溶液吸收多余的氯气;
故答案为吸收氯气,防止污染。

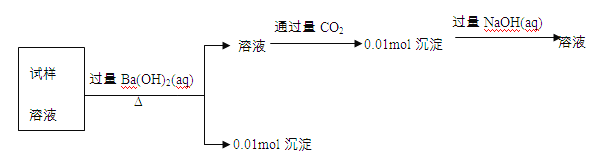
【题目】PdCl2广泛用作催化剂和一些物质的检测试剂。由Pd(NH3)2Cl2制备PdCl2工艺流程如图所示。

(1)肼(N2H4)可以被看作二元弱碱,结合质子生成N2H5+或N2H62+。肼与少量稀硫酸混合后,得到产物的化学式为___。
(2)对工艺流程图中的滤液处理办法最好的是:___
a.返到提钯废液中,循环使用 b.转化为无毒物质后排放 c.深埋于地下
(3)王水溶钯时,Pd被氧化为H2PdCl4。同时得到唯一还原产物亚硝酰氯(NOCl)。反应消耗的HCl与HNO3的物质的量之比为___。
(4)赶硝,是将残余的NO3浓度降低到不大于0.04%。实验数据记录如表:
表一:不同HCl用量和MxOy用量(每10gPd)与NO3残留量
HCl用量(mL) | MxOy用量(mL) | NO3含量(%) |
5 | 0、10、20、30、40 | 0.15、0.10、0.05、0.04、0.03 |
10 | 0、5、10、15、20 | 0.10、0.08、0.05、0.03、0.02 |
15 | 0、5、10、15、20 | 0.08、0.06、0.05、0.03、0.02 |
处理1吨Pd,需要用到HCl和MxOy的总体积至少为___m3(合理选择表格里相关数据计算)。
(5)煅烧过程发生分解反应,化学方程式为:___。
(6)浸有磷钼酸铵溶液的氯化钯试纸遇微量CO立即变成蓝色。原理较为复杂,第一步是CO还原PdCl2得到Pd单质,同时有常见的氧化物生成。写出反应原理中第一步的化学方程式:___