题目内容
【题目】氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。
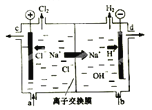
完成下列填空:
(1).写出电解饱和食盐水的离子方程式 。
(2).离子交换膜的作用为: 、 。
(3).精制饱和食盐水从图中 位置补充,氢氧化钠溶液从图中 位置流出。(选填“a”、“b”、“c”或“d”)
(4).KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式 。
【答案】(1)2Cl-+2H2O![]() Cl2↑+H2↑+2OH-。
Cl2↑+H2↑+2OH-。
(2)阻止OH-进入阳极室,与Cl2发生副反应;避免氯气与氢气反应。
(3)a;d;(4)2KClO3+ H2C2O4+ 2H2SO4= 2ClO2+2CO2+2KHSO4+2H2O.
【解析】
试题分析:(1)电解饱和食盐水时,溶液中的阳离子H+在阴极得到电子生成H2逸出,使附近的水溶液显碱性,溶液中的阴离子Cl-在阳极失去电子,发生氧化反应生成Cl2,反应的离子方程式是2Cl-+2H2O![]() Cl2↑+H2↑+2OH-。
Cl2↑+H2↑+2OH-。
(2)图中的离子交换膜只允许阳离子通过,是阳离子交换膜,允许阳离子通过,但不能使阴离子通过,这样就可以阻止阴极溶液中的OH-进入阳极室,与氯气发生反应,阻止Cl-进入阴极室,使在阴极区产生的NaOH纯度更高,同时可以阻止阳极产生的Cl2和阴极产生的H2混合发生爆炸,所以离子交换膜的作用为:阻止OH-进入阳极室,与Cl2发生副反应;避免氯气与氢气反应。
(3)随着电解的进行,溶质NaCl不断消耗,所以应该及时补充,精制饱和食盐水从与阳极连接的图中a位置补充,由于阴极H+不断放电,附近的溶液显碱性,氢氧化钠溶液从图中d位置流出。
(4)KClO3有氧化性,H2C2O4有还原性,在酸性条件下KClO3可以和草酸(H2C2O4)生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质,根据电子守恒及原子守恒,可得该反应的化学方程式是2KClO3+ H2C2O4+ 2H2SO4= 2ClO2+2CO2+2KHSO4+2H2O。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案